|
|
|
用0.2mol/L HCl溶液滴定0.2mol/L NaOH,如果到达滴定的终点时不?【水的电离平衡】
2016-12-25 18:21:11
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 用0.2mol/L HCl溶液滴定0.2mol/L NaOH,如果到达滴定的终点时不慎多加了1滴盐酸溶液(1滴溶液的体积约为0.05mL),继续加水至100mL,所得溶液的pH是
A.4
B.1
C.10
D. 3.3
|
选择题 用0.2mol/L HCl溶液滴定0.2mol/L NaOH,如果到达滴定的终点时不慎多加了1滴盐酸溶液(1滴溶液的体积约为0.05mL),继续加水至100mL,所得溶液的pH是
A.4
B.1
C.10
D.3.3
|
本题答案:A
本题解析:
试题分析:如果到达滴定的终点时不慎多加了1滴盐酸溶液(1滴溶液的体积约为0.05mL),则盐酸过量,溶液显酸性,所以反应后溶液中氢离子浓度=
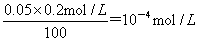
,则pH=4,答案选A。
考点:考查溶液pH的计算
点评:该题是高考中的常见题型和考点,属于中等难度试题的考查。在注 重对学生基础知识巩固和训练的同时,侧重对学生答题能力的培养和训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和应试能力。
本题所属考点:【水的电离平衡】
本题难易程度:【一般】
The last drop makes the cup run over. 满斟之杯,溢于最后一滴.
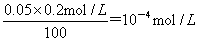 ,则pH=4,答案选A。
,则pH=4,答案选A。