|
|
|
HA为酸性略强于醋酸的一元弱酸,则下列叙述正确的是A.0. 1【水的电离平衡】
2016-12-25 18:22:34
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 HA为酸性略强于醋酸的一元弱酸,则下列叙述正确的是
A.0. 1 mol?L-1 HA中c(H+)= c(OH-)+ c(A-)
B.0. 1 mol?L-1 HA与 0. 1 mol?L-1NaOH 混合至溶液呈中性:c(Na+)= c(A-)
C.0. 1 mol?L-1 NaA 中c(Na+)> c(OH-)>c(A-)> c(H+)
D.0. 1 mol?L-1 HA中加入少量NaA固体,HA的电离常数减小
|
选择题 HA为酸性略强于醋酸的一元弱酸,则下列叙述正确的是
A.0. 1 mol?L-1 HA中c(H+)= c(OH-)+ c(A-)
B.0. 1 mol?L-1 HA与 0. 1 mol?L-1NaOH 混合至溶液呈中性:c(Na+)= c(A-)
C.0. 1 mol?L-1 NaA 中c(Na+)> c(OH-)>c(A-)> c(H+)
D.0. 1 mol?L-1 HA中加入少量NaA固体,HA的电离常数减小
|
本题答案:AB
本题解析:
试题分析:依题意,HA
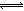
H++A―、H2O
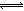
H++OH―,则稀HA溶液中含有A―、OH―、H+,溶液呈电中性,则阴阳离子所带正负电荷总浓度相等,即c(A-)+ c(OH-) = c(H+),故A选项正确;酸碱中和反应后所得溶液中含有A―、OH―、Na+、H+,溶液呈电中性,则阴阳离子所带正负电荷总浓度相等,即c(A-)+c(OH-)=c(Na+)+c(H+),若溶液呈电中性,则c(A-) =c(Na+),故B选项正确;NaA=Na++A―、H2O
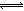
H++OH―,钠离子不能水解,少部分A―能水解生成HA,消耗水电离出的氢离子,促进水的电离,则稀盐溶液中c(Na+)>c(A-)>c(OH-)>c(H+),故C选项错误;稀HA溶液中存在电离平衡:HA
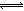
H++A―,NaA是强电解质,加入NaA固体,其完全电离出的A―增大溶液中c(A-),增大生成物浓度使弱酸电离平衡向逆反应方向移动,但HA的电离平衡常数只与温度有关,温度不变电离平衡常数不变,故D选项错误。
考点:考查水溶液中粒子浓度大小关系,涉及弱酸溶液或弱酸与强碱混合溶液中的电荷守恒关系式、酸性的酸碱性、盐溶液中离子浓度大小顺序、弱酸电离平衡的移动规律、弱酸电离平衡常数的影响因素及规律等。
本题所属考点:【水的电离平衡】
本题难易程度:【困难】
An ounce of prevention is worth a pound of cure. 一分预防胜过十分治疗。
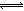 H++A―、H2O
H++A―、H2O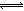 H++OH―,则稀HA溶液中含有A―、OH―、H+,溶液呈电中性,则阴阳离子所带正负电荷总浓度相等,即c(A-)+ c(OH-) = c(H+),故A选项正确;酸碱中和反应后所得溶液中含有A―、OH―、Na+、H+,溶液呈电中性,则阴阳离子所带正负电荷总浓度相等,即c(A-)+c(OH-)=c(Na+)+c(H+),若溶液呈电中性,则c(A-) =c(Na+),故B选项正确;NaA=Na++A―、H2O
H++OH―,则稀HA溶液中含有A―、OH―、H+,溶液呈电中性,则阴阳离子所带正负电荷总浓度相等,即c(A-)+ c(OH-) = c(H+),故A选项正确;酸碱中和反应后所得溶液中含有A―、OH―、Na+、H+,溶液呈电中性,则阴阳离子所带正负电荷总浓度相等,即c(A-)+c(OH-)=c(Na+)+c(H+),若溶液呈电中性,则c(A-) =c(Na+),故B选项正确;NaA=Na++A―、H2O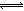 H++OH―,钠离子不能水解,少部分A―能水解生成HA,消耗水电离出的氢离子,促进水的电离,则稀盐溶液中c(Na+)>c(A-)>c(OH-)>c(H+),故C选项错误;稀HA溶液中存在电离平衡:HA
H++OH―,钠离子不能水解,少部分A―能水解生成HA,消耗水电离出的氢离子,促进水的电离,则稀盐溶液中c(Na+)>c(A-)>c(OH-)>c(H+),故C选项错误;稀HA溶液中存在电离平衡:HA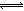 H++A―,NaA是强电解质,加入NaA固体,其完全电离出的A―增大溶液中c(A-),增大生成物浓度使弱酸电离平衡向逆反应方向移动,但HA的电离平衡常数只与温度有关,温度不变电离平衡常数不变,故D选项错误。
H++A―,NaA是强电解质,加入NaA固体,其完全电离出的A―增大溶液中c(A-),增大生成物浓度使弱酸电离平衡向逆反应方向移动,但HA的电离平衡常数只与温度有关,温度不变电离平衡常数不变,故D选项错误。