|
|
|
常温下,对于1L0.005mol・L-1硫酸表述中正确的是A.由水电?【水的电离平衡】
2016-12-25 18:26:38
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 常温下,对于1L0.005mol・L-1硫酸表述中正确的是
A.由水电离出的c(H+)=1.0×10-12mo l・L-1
B.加水稀释后,溶液中所有离子的浓度均减少
C.2c(H+)= c(SO42-)+ c(OH-)
D.滴加稀氨水使pH=7,则c(NH4+)=" 2" c(SO42-)
|
选择题 常温下,对于1L0.005mol・L-1硫酸表述中正确的是
A.由水电离出的c(H+)=1.0×10-12mol・L-1
B.加水稀释后,溶液中所有离子的浓度均减少
C.2c(H+)= c(SO42-)+ c(OH-)
D.滴加稀氨水使pH=7,则c(NH4+)=" 2" c(SO42-)
|
本题答案:AD
本题解析:
试题分析:硫酸是强酸,能完全电离,则H2SO4=2H++SO42―中氢离子浓度与硫酸浓度之比等于系数之比,即c(H+)=0.005mol・L-1×2 =0.01mol/L,由于水是极弱电解质,硫酸能抑制水的电离,水电离出的氢离子可忽略不计,则溶液中c(H+)=0.01mol/L,由于常温下水的离子积为1.0×10-14,则溶液中c(OH-)=Kw/ c(H+)=1.0×10-12 mol/L,由于溶质不能电离出氢氧根离子,氢氧根离子全部来自水的电离,则水电离出c(OH-)= 1.0×10-12 mol/L,由于H2O
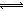
H++OH―中氢离子和氢氧根离子的浓度之比等于系数之比,则由水电离出的c(H+)=1.0×10-12mol・L-1,故A正确;硫酸溶液呈酸性,加水稀释后,酸性减弱,氢离子、硫酸根离子浓度均减小,但温度不变水的离子积不变,即溶液中氢离子浓度与氢氧根离子浓度的乘积不变,所以溶液中氢氧根离子浓度一定增大,故B错;硫酸溶液中含有氢离子、硫酸根离子和氢氧根离子,根据电荷守恒原理可得:c(H+)="2" c(SO42-)+ c(OH-),故C错;无论量的多少,稀硫酸与氨水混合后溶液只有铵根离子、氢离子、硫酸根离子和氢氧根离子,根据电荷守恒规律可得:c(NH4+)+c(H+)="2" c(SO42-)+ c(OH-),由于滴加稀氨水使pH=7,则该溶液中c(NH4+)="2" c(SO42-),故D正确。
考点:考查水溶液中的离子浓度大小关系,涉及物质的量浓度、强酸电离方程式中氢离子与强酸的 系数之比的应用、水的电离、水的离子积、溶液中氢氧根离子浓度的计算、强酸溶液中水电离出的氢离子浓度的计算、强酸溶液中存在的离子、强酸稀释后离子浓度大小变化情况、电荷守恒原理及其应用、溶液的酸碱性与pH等。
本题所属考点:【水的电离平衡】
本题难易程度:【一般】
Know something of everything and everything of something. 通百艺而精于一.
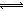 H++OH―中氢离子和氢氧根离子的浓度之比等于系数之比,则由水电离出的c(H+)=1.0×10-12mol・L-1,故A正确;硫酸溶液呈酸性,加水稀释后,酸性减弱,氢离子、硫酸根离子浓度均减小,但温度不变水的离子积不变,即溶液中氢离子浓度与氢氧根离子浓度的乘积不变,所以溶液中氢氧根离子浓度一定增大,故B错;硫酸溶液中含有氢离子、硫酸根离子和氢氧根离子,根据电荷守恒原理可得:c(H+)="2" c(SO42-)+ c(OH-),故C错;无论量的多少,稀硫酸与氨水混合后溶液只有铵根离子、氢离子、硫酸根离子和氢氧根离子,根据电荷守恒规律可得:c(NH4+)+c(H+)="2" c(SO42-)+ c(OH-),由于滴加稀氨水使pH=7,则该溶液中c(NH4+)="2" c(SO42-),故D正确。
H++OH―中氢离子和氢氧根离子的浓度之比等于系数之比,则由水电离出的c(H+)=1.0×10-12mol・L-1,故A正确;硫酸溶液呈酸性,加水稀释后,酸性减弱,氢离子、硫酸根离子浓度均减小,但温度不变水的离子积不变,即溶液中氢离子浓度与氢氧根离子浓度的乘积不变,所以溶液中氢氧根离子浓度一定增大,故B错;硫酸溶液中含有氢离子、硫酸根离子和氢氧根离子,根据电荷守恒原理可得:c(H+)="2" c(SO42-)+ c(OH-),故C错;无论量的多少,稀硫酸与氨水混合后溶液只有铵根离子、氢离子、硫酸根离子和氢氧根离子,根据电荷守恒规律可得:c(NH4+)+c(H+)="2" c(SO42-)+ c(OH-),由于滴加稀氨水使pH=7,则该溶液中c(NH4+)="2" c(SO42-),故D正确。