微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (10分)Na2S2O3可用作照相的定影剂等。已知Na2S2O3的某些性质如下:
①S2O32-能被I2氧化为无色的S4O62-;
②酸性条件下S2O32-迅速分解为S和SO2
I.市售Na2S2O3中常含有SO42-,请完成以下方案,检验其中含有的SO42-:
实验步骤
| 预期现象或结论
|
步骤1:取少量固体样品溶于无氧蒸馏水中
| 固体完全溶解得无色澄清溶液
|
步骤2:加入过量盐酸
|
|
步骤3:
| 有白色沉淀产生,说明样品中含有SO42-
|
Ⅱ.利用K2Cr2O7标准溶液可以定量测定市售硫代硫酸钠试剂的纯度,步骤为:
①溶液配制:称取1.000gNa2S2O3试样,用新煮沸并冷却 的蒸馏水溶解,最终定容至100mL。
②滴定:取10.00mL 0.01000mol・L-1 K2Cr2O7标准溶液,加硫酸酸化,再加过量KI溶液。
③往步骤②所得溶液加入淀粉作指示剂,用Na2S2O3滴定至终点(2S2O32-+ I2="==" S4O62-+ 2I-),记录Na2S2O3溶液用量,平行滴定3次。
(1)步骤①中必须使用的玻璃仪器有烧杯、玻璃棒、 和 。
(2)完成并配平步骤②中的离子反应:
Cr2O72- + ( ) + I- === I2 + Cr3+ + H2O
(3)若3次滴定Na2S2O3溶液的平均用量为12.00mL,则样品的纯度为 (保留两位有效数字)。
填空题 (10分)Na2S2O3可用作照相的定影剂等。已知Na2S2O3的某些性质如下:
①S2O32-能被I2氧化为无色的S4O62-;
②酸性条件下S2O32-迅速分解为S和SO2
I.市售Na2S2O3中常含有SO42-,请完成以下方案,检验其中含有的SO42-:
实验步骤
| 预期现象或结论
|
步骤1:取少量固体样品溶于无氧蒸馏水中
| 固体完全溶解得无色澄清溶液
|
步骤2:加入过量盐酸
|
|
步骤3:
| 有白色沉淀产生,说明样品中含有SO42-
|
Ⅱ.利用K2Cr2O7标准溶液可以定量测定市售硫代硫酸钠试剂的纯度,步骤为:
①溶液配制:称取1.000gNa2S2O3试样,用新煮沸并冷却的蒸馏水溶解,最终定容至100mL。
②滴定:取10.00mL 0.01000mol・L-1 K2Cr2O7标准溶液,加硫酸酸化,再加过量KI溶液。
③往步骤②所得溶液加入淀粉作指示剂,用Na2S2O3滴定至终点(2S2O32-+ I2="==" S4O62-+ 2I-),记录Na2S2O3溶液用量,平行滴定3次。
(1)步骤①中必须使用的玻璃仪器有烧杯、玻璃棒、 和 。
(2)完成并配平步骤②中的离子反应:
Cr2O72- + ( ) + I- === I2 + Cr3+ + H2O
(3)若3次滴定Na2S2O3溶液的平均用量为12.00mL,则样品的纯度为 (保留两位有效数字)。
本题答案:Ⅰ.
实验步骤
预期现象或结论
本题解析:
试题分析:Ⅰ.由于Na2S2O3会干扰硫酸根的检验,所以要检验硫酸根是否存在,则首先要把硫代硫酸钠转化为S和SO2,然后再检验硫酸根的存在。
(1)步骤①是配制100ml溶液,则必须使用的玻璃仪器除烧杯、玻璃棒外还有100mL容量瓶、胶头滴管。
(2)zau反应中碘元素的化合价从―1价升高到0价失去1个电子,Cr元素的化合价从+6价降低到+3价,达到3个电子,则根据电子得失守恒可知氧化剂与还原剂的物质的量之比是1:6,则配平后的方程式外Cr2O72- + 14H+ +6I- =3I2 + 2Cr3+ + 7H2O.
(3)根据方程式可知K2Cr2O7~3I2~6 Na2S2O3,若3次滴定Na2S2O3溶液的平均用量为12.00mL,则硫代硫酸钠的浓度是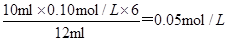 ,所以样品的纯度为
,所以样品的纯度为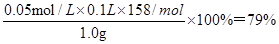 。
。
考点:考查物质检验、含量测定实验方案设计与探究
本题所属考点:【水的电离平衡】
本题难易程度:【一般】
Painting is silent poetry,and poetry is a speaking picture. 画是无言之诗,诗是有声之画。