微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 某温度时,在25mL 0.1mol/L NaOH溶液中逐滴加入0.2mol/L CH3COOH溶液,曲线如图所示,有关粒子浓度关系的比较正确的是
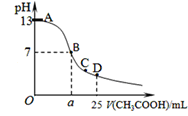
A.在D点:c(CH3COO-)+c(CH3COOH)=2c(Na+)
B.在C点:c(CH3COO-)>c(Na+)>c(O来源:91考试网 91ExAm.orgH-)>c(H+)
C.在B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
D.在A、B间任一点,溶液中一定都有c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
选择题 某温度时,在25mL 0.1mol/L NaOH溶液中逐滴加入0.2mol/L CH3COOH溶液,曲线如图所示,有关粒子浓度关系的比较正确的是

A.在D点:c(CH3COO-)+c(CH3COOH)=2c(Na+)
B.在C点:c(CH3COO-)>c(Na+)>c(OH -)>c(H+)
C.在B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
D.在A、B间任一点,溶液中一定都有c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
本题答案:A
本题解析:
试题分析:A项是物料守恒,对;B项、C点溶液显酸性,c(H+)>c(OH-),错;C项、在B点溶液显中性c(Na+)=c(CH3COO-)>c(OH-)=c(H+),错;在A、B间任一点,不一定有c(CH3COO-)>c(OH-),反应开始时c(OH-)比较大,错,选A。
考点:酸碱中和过程中溶液中的离子浓度比较。
本题所属考点:【水的电离平衡】
本题难易程度:【一般】
Lazy folk take the most pains. 懒人躲懒最费力.