|
|
|
27.(10分)下图为某加碘盐标签的一部分。<img src="http:/【水的电离平衡】
2016-12-25 19:38:02
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 27.(10分)下图为某加碘盐标签的一部分。

已知:①KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O
②I2+2Na2S2 O3=2NaI+Na2S4O6(无色)
某同学想定量测定此加碘盐中碘元素的含量,进行以下实验:
步骤1:称取ag市售食盐,配成溶液,全部转移至锥形瓶中,
加入适量新制KI溶液,滴入几滴稀硫酸,溶液变黄色,再加入3滴淀粉溶液。
步骤2:取一支50mL碱式滴定管,用bmol・L-1的新制Na2S2O3 溶液润洗2~3次后,装满溶液,调节液面高度至0刻度。
步骤3:开始滴定直至终点,重复操作2~3次,实验数据记录如下:
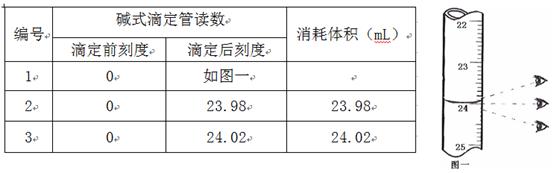
(1)第一次读数为 mL。
(2)滴定终点的判断方法 。
(3)经过计算,此碘盐碘元素的含量为 mg・kg-1(用含a、b的最简表达式表示) 。
(4)下列操作可能会导致测量结果偏低的是 。
A.步骤1中称取食盐时将砝码放在左盘,食盐放在放在右盘,游码读数为0.5g
B.步骤1所配食盐溶液未完全转移至锥形瓶
C.步骤2中滴定管洗涤后未润洗
D.步骤3滴定前滴定管尖嘴处有气泡,滴定后气泡消失
| (5)请在答题纸的方框内画出正在排气泡的碱式滴定管(仅画出刻度以下部分)
填空题 27.(10分)下图为某加碘盐标签的一部分。

已知:①KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O
②I2+2Na2S2O3=2NaI+Na2S4O6(无色)
某同学想定量测定此加碘盐中碘元素的含量,进行 以下实验:
步骤1:称取ag市售食盐,配成溶液,全部转移至锥形瓶中,
加入适量新制KI溶液,滴入几滴稀硫酸,溶液变黄色,再加入3滴淀粉溶液。
步骤2:取一支50mL碱式滴定管,用bmol・L-1的新制Na2S2O3 溶液润洗2~3次后,装满溶液,调节液面高度至0刻度。
步骤3:开始滴定直至终点,重复操作2~3次,实验数据记录如下:

(1)第一次读数为 mL。
(2)滴定终点的判断方法 。
(3)经过计算,此碘盐碘元素的含量为 mg・kg-1(用含a、b的最简表达式表示) 。
(4)下列操作可能会导致测量结果偏低的是 。
A.步骤1中称取食盐时将砝码放在左盘,食盐放在放在右盘,游码读数为0.5g
B.步骤1所配食盐溶液未完全转移至锥形瓶
C.步骤2中滴定管洗涤后未润洗
D.步骤3滴定前滴定管尖嘴处有气泡,滴定后气泡消失
|
(5)请在答题纸的方框内画出正在排气泡的碱式滴定管(仅画出刻度以下部分)
本题答案:(1)24.00
(2)溶液颜色恰好由蓝色变为无色且半
本题解析:
试题分析:正确读取读数,目光平视,刻度为24.00ml;滴定终点的判断,当变色稳定,半分钟不变色时说明达到滴定重点;碘盐碘点元素的含量用碘酸钾的质量与碘元素的质量分数相乘,逐步计算ω=
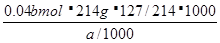
=508000b/a;滴定时滴定管未润洗,结果偏大;滴定管尖嘴处有气泡,体积读数变大,结果偏大。
考点:滴定原理及应用
点评:要掌握酸碱滴定的基本步骤,扩展到普通滴定,会进行误差的分析,正确判断滴定的终点。
本题所属考点:【水的电离平衡】
本题难易程度:【困难】
As devotion unites lovers so perfidy estranges friends. 忠诚是爱情的桥梁,欺诈是友谊的敌人.
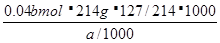 =508000b/a;滴定时滴定管未润洗,结果偏大;滴定管尖嘴处有气泡,体积读数变大,结果偏大。
=508000b/a;滴定时滴定管未润洗,结果偏大;滴定管尖嘴处有气泡,体积读数变大,结果偏大。