|
|
|
室温时,向20 mL 0.1 mol・L-1NH4HSO4溶液中滴加0.1 mol・L-1N【水的电离平衡】
2016-12-25 19:44:49
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 室温时,向20 mL 0.1 mol・L-1NH4HSO4溶液中滴加0.1 mol・L-1NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示(假设滴加过程中无气体产生,且混合溶液的体积可看成混合前两溶液的体积之和),下列说法不正确的是:
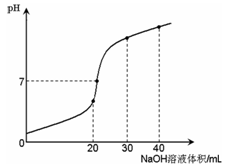
A.PH=7时,溶液中c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)
B.当V(NaOH)=20mL时,溶液中水的电离程度比纯水大
C.当V(NaOH)=30mL时,溶液中 c(SO42-)+ c(H+)="=" c(NH3・H2O) + c(OH-)
D.滴加NaOH溶液从30mL至40mL,溶液中Na+与SO42-浓度之和始终为0.1 mol・L-1
|
选择题 室温时,向20 mL 0.1 mol・L-1NH4HSO4溶液中滴加0.1 mol・L-1NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示(假设滴加过程中无气体产生,且混合溶液的体积可看成混合前两溶液的体积之和),下列说法不正确的是:

A.PH=7时,溶液中c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)
B.当V(NaOH)=20mL时,溶液中水的电离程度比纯水大
C.当V(NaOH)=30mL时,溶液中 c(SO42-)+ c(H+)="=" c(NH3・H2O) + c(OH-)
D.滴加NaOH溶液从30mL至40mL,溶液中Na+与SO42-浓度之和始终为0.1 mol・L-1
|
本题答案:C
本题解析:
试题分析:A、pH=7时,溶液呈中性,c(OH-)=c(H+),根据电荷守恒,则2c(SO42-)+ c(OH-)=c(H+)+ c(NH4+)+ c(Na+),2c(SO42-)=c(NH4+)+ c(Na+),此时氢氧化钠溶液的体积大于20mL,则c(Na+)>c(SO42-),所以c(SO42-)>c(NH4+),正确;B、当V(NaOH)=20mL时,氢氧化钠与硫酸氢铵的物质的量相同,则生成硫酸钠和硫酸铵的混合液,铵根离子的水解使溶液中水的电离程度比纯水大,正确;C、当V(NaOH)=30mL时,钠离子的物质的量是硫酸根离子或N元素物质的量的1.5倍,根据元素守恒c(Na+)=1.5[c(NH3・H2O)+ c(NH4+)]="1.5" c(SO42-),根据电荷守恒,则2c(SO42-)+ c(OH-)=c(H+)+ c(NH4+)+ c(Na+),所以将钠离子和铵根离子消去,得溶液中0.5 c(SO42-)+ c(H+)="=" c(NH3・H 2O) + c(OH-),错误;D、因为硫酸根离子与钠离子都不发生水解反应,原溶液中硫酸根离子与钠离子的浓度相等,都是0.1mol/L,所以无论溶液的体积是多少,二者混合后溶液的总体积是相同的,则溶液中Na+与SO42-浓度之和始终为0.1 mol・L-1,正确,答案选C。
考点:考查电解质溶液混合的计算,离子浓度的比较
本题所属考点:【水的电离平衡】
本题难易程度:【困难】
Man proposes, God disposes. 谋事在人,戒事在天。