|
|
|
常温下向盛水烧杯中加2g生石灰(如下图)。搅拌后再恢复到原温,【水的电离平衡】
2016-12-25 19:45:16
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 常温下向盛水烧杯中加2g生石灰(如下图)。搅拌后再恢复到原温,在此过程中,下列说法正确的是
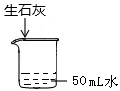
A.水的电离常数不变
B.Ca(OH)2的电离程度先大后变小然最 后不变
C.水的电离平衡向逆反应方向移动最后不变
D.水的电离度将会先变小然后变大最后不变
|
选择题 常温下向盛水烧杯中加2g生石灰(如下图)。搅拌后再恢复到原温,在此过程中,下列说法正确的是

A.水的电离常数不变
B.Ca(OH)2的电离程度先大后变小然最后不变
C.水的电离平衡向逆反应方向移动最后不变
D.水的电离度将会先变小然后变大最后不变
|
本题答案:C
本题解析:
试题分析:A、CaO与水反应生成氢氧化钙,使温度升高,则水的电离常数先增大,后又恢复到原温度,则水的电离常数又减小,所以反应过程中,水的电离常数发生变化,错误; B、2gCaO加入到50mL水中,形成氢氧化钙溶液,氢氧化钙完全电离,不存在电离程度大小的问题,错误;C、因为 溶液的浓度较稀,该反应放热,温度升高,水的电离正向移动,而生成氢氧化钙使溶液中氢氧根离子浓度增大,水的电离逆向移动,最终恢复到原温度后水的电离平衡逆向移动,正确;D、在反应过程中,温度升高对水电离的影响大于氢氧根离子的浓度变化对水电离的影响,所以开始水的电离度会增大,后恢复到原温度,则平衡逆向进行,水的电离度又减小最后不变,错误,答案选C。
考点:考查对水的电离平衡的影响
本题所属考点:【水的电离平衡】
本题难易程度:【一般】
Open different locks with different keys. 一把钥匙开一把锁。