微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (16分)醋酸是一种常见的弱酸。
(1)假如某醋酸溶液中c(CH3COOH)=0.10mol/L,c(H+)=1.3×10-3mol/L,则此时c(CH3COO-)约为
mol/L;计算此时醋酸的电离平衡常数,写出计算过程。[注: c平衡(CH3COOH)≈0.10mol/L,水的电离可忽略不计]
(2)为了探究镁条与盐酸、醋酸反应时,浓度或温度对反应速率(观察镁条消失的时间)的影响,准备了以下化学用品:0.20 mol・L-1与0.40 mol・L-1的HCl溶液、0.20 mol・L-1与0.40 mol・L-1的CH3COOH溶液、4条镁条(形状、大小、质量相同)、几支试管和胶头滴管,酸液温度控制为298 K和308 K。
①酸液都取足量、相同体积,请你帮助完成以下实验设计表:
实验
编号
| 温度
(K)
| 盐酸浓度
(mol・L-1)
| 醋酸浓度
(mol・L-1)
| 实验目的
|
a
| 298
| 0.20
|
| I.实验a和b是探究 对镁与盐酸反应速率的影响;
II.实验a和c是探究 对镁与盐酸反应速率的影响;
III.实验a和d是探究相同温度下,相同浓度的盐酸、醋酸与镁反应速率的区别
|
b
| 308
| 0.20
|
|
c
| 298
| 0.40
|
|
d
|
|
|
|
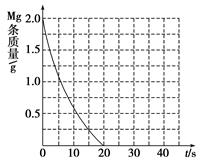
②若①中实验a镁条消失的时间是20 s,则镁条剩余质量与时间关系图如下图。假设:该反应温度每升高10 ℃,反应速率是原来的2倍;温度相同时,醋酸是相同浓度盐酸平均速度的1/2,请在此图中大致画出“实验b”、“实验d”的镁条剩余质量与时间关系曲线,请注意必要的标注。
(3)镁及其化合物在生产和生活中有着广泛的应用,依据镁的性质、用途等回答下列问题:
已知:①Mg(s)+2H2O(g)===Mg(OH)2(s)+H2(g) ΔH1=-441 kJ・mol-1
②H2O(g)===H2(g)+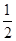 O2(g) ΔH2=+242 kJ・mol-1
O2(g) ΔH2=+242 kJ・mol-1
③Mg(s)+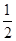 O2(g)===MgO(s) ΔH3=-602 kJ・mol-1。
O2(g)===MgO(s) ΔH3=-602 kJ・mol-1。
则氢氧化镁分解的热化学方程式是 。
填空题 (16分)醋酸是一种常见的弱酸。
(1)假如某醋酸溶液中c(CH3COOH)=0.10mol/L,c(H+)=1.3×10-3mol/L,则此时c(CH3COO-)约为
mol/L;计算此时醋酸的电离平衡常数,写出计算过程。[注: c平衡(CH3COOH)≈0.10mol/L,水的电离可忽略不计]
(2)为了探究镁条与盐酸、醋酸反应时,浓度或温度对反应速率(观察镁条消失的时间)的影响,准备了以下化学用品:0.20 mol・L-1与0.40 mol・L-1的HCl溶液、0.20 mol・L-1与0.40 mol・L-1的CH3COOH溶液、4条镁条(形状、大小、质量相同)、几支试管和胶头滴管,酸液温度控制为298 K和308 K。
①酸液都取足量、相同体积,请你帮助完成以下实验设计表:
实验
编号
| 温度
(K)
| 盐酸浓度
(mol・L-1)
| 醋酸浓度
(mol・L-1)
| 实验目的
|
a
| 298
| 0.20
|
| I.实验a和b是探究 对镁与盐酸反应速率的影响;
II.实验a和c是探究 对镁与盐酸反应速率的影响;
III.实验a和d是探究相同温度下,相同浓度的盐酸、醋酸与镁反应速率的区别
|
b
| 308
| 0.20
|
|
c
| 298
| 0.40
|
|
d
|
|
|
|
②若①中实验a镁条消失的时间是20 s,则镁条剩余质量与时间关系图如下图。假设:该反应温度每升高10 ℃,反应速率是原来的2倍;温度相同时,醋酸是相同浓度盐酸平均速度的1/2,请在此图中大致画出“实验b”、“实验d”的镁条剩余质量与时间关系曲线,请注意必要的标注。

(3)镁及其化合物在生产和生活中有着广泛的应用,依据镁的性质、用途等回答下列问题:
已知:①Mg(s)+2H2O(g)===Mg(OH)2(s)+H2(g) ΔH1=-441 kJ・mol-1
②H2O(g)===H2(g)+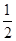 O2(g) ΔH2=+242 kJ・mol-1
O2(g) ΔH2=+242 kJ・mol-1
③Mg(s)+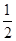 O2(g)===MgO(s) ΔH3=-602 kJ・mol-1。
O2(g)===MgO(s) ΔH3=-602 kJ・mol-1。
则氢氧化镁分解的热化学方程式是 。
本题答案:(1) 1.3×10-3 (1分);
本题解析:
试题分析:(1)某醋酸溶液中c(CH3COOH)=0.10mol/L,CH3COOH  CH3COO-+ H+;c(H+)=" 1.3×" 10-3mol/L ,则此时c(CH3COO-)= c(H+)=1.3×10-3mol/L;此时醋酸的电离平衡常数
CH3COO-+ H+;c(H+)=" 1.3×" 10-3mol/L ,则此时c(CH3COO-)= c(H+)=1.3×10-3mol/L;此时醋酸的电离平衡常数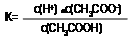 ="(" 1.3×10-3)2/0.10 mol/L=1.7×10-5 mol/L(2)①Ⅰ、反应的其他条件相同,而温度不同,因此实验a和b是探究温度对镁与盐酸反应速率的影响;II.实验a和c的温度相同we盐酸的浓度不相同,因此实验a和c是探究浓度对镁与盐酸反应速率的影响;III.实验a和d是探究相同温度下,相同浓度的盐酸、醋酸与镁反应速率的区别,所以实验d的反应温度是298,盐酸与醋酸的浓度0.20mol/L;②若①中实验a镁条消失的时间是20 s,则镁条剩余质量与时间关系图如图。假设:该反应温度每升高10 ℃,反应速率是原来的2倍;温度相同时,醋酸是相同浓度盐酸平均速度的1/2,则在此图中大致画出“实验b”、“实验d”的镁条剩余质量与时间关系曲线如下图,
="(" 1.3×10-3)2/0.10 mol/L=1.7×10-5 mol/L(2)①Ⅰ、反应的其他条件相同,而温度不同,因此实验a和b是探究温度对镁与盐酸反应速率的影响;II.实验a和c的温度相同we盐酸的浓度不相同,因此实验a和c是探究浓度对镁与盐酸反应速率的影响;III.实验a和d是探究相同温度下,相同浓度的盐酸、醋酸与镁反应速率的区别,所以实验d的反应温度是298,盐酸与醋酸的浓度0.20mol/L;②若①中实验a镁条消失的时间是20 s,则镁条剩余质量与时间关系图如图。假设:该反应温度每升高10 ℃,反应速率是原来的2倍;温度相同时,醋酸是相同浓度盐酸平均速度的1/2,则在此图中大致画出“实验b”、“实验d”的镁条剩余质量与时间关系曲线如下图,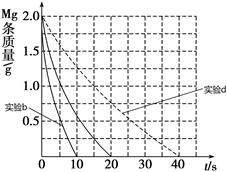 。(3)②+③-①,整理可得:Mg(OH)2(s)===MgO(s)+H2O(g) ΔH=+81 kJ/mol。
。(3)②+③-①,整理可得:Mg(OH)2(s)===MgO(s)+H2O(g) ΔH=+81 kJ/mol。
考点:考查弱电解质的电离平衡、电离平衡常数的计算、影响速率的各种因素的图像法表示、盖斯定律的应用、热化学 的书写的知识。
本题所属考点:【弱电解质电离平衡】
本题难易程度:【困难】
Joy is found only is Love, Life is found only in loving. 只有在爱中才能找到欢乐,只有在爱别人中才能找到生活.