|
|
|
常温下,将0.2 mol・L-1的一元酸HA溶液和0.1 mol・L-1的NaOH溶【弱电解质电离平衡】
2016-12-25 23:15:24
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 常温下,将0.2 mol・L-1的一元酸HA溶液和0.1 mol・L-1的NaOH溶液等体积混合后,pH大于7,若混合后溶液体积等于两溶液体积之和,则下列关系中正确的是
| A.[HA]<[A-] | B.[HA]一定大于0.1 mol・L-1
| | C.[Na+]=[HA]+ [A-] | D.2[OH-]=2[H+]+[HA]-[A-]
|
选择题 常温下,将0 .2 mol・L-1的一元酸HA溶液和0.1 mol・L-1的NaOH溶液等体积混合后,pH大于7,若混合后溶液体积等于两溶液体积之和,则下列关系中正确的是
| A.[HA]<[A-] | B.[HA]一定大于0.1 mol・L-1
|
| C.[Na+]=[HA]+[A-] | D.2[OH-]=2[H+]+[HA]-[A-]
|
本题答案:D
本题解析:
试题分析:0.2 mol・L-1的一元酸HA溶液和0.1 mol・L-1的NaOH溶液等体积混合后,生成等物质的量的NaA、HA;
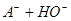
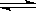
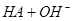
,
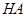
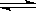
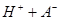
;pH大于7,说明水解大于电离,所以[HA]>[A-] ,故A错误;[HA]一定大于0.05 mol・L-1 ,故B错误;根据物料守恒,2[Na+]="[HA]+[A-]" ,故C错误; 根据电荷守恒和物料守恒,2[OH-]=2[H+]+[HA]-[A-],故D正确。
考点:本题考查弱电解质电离和盐的水解。
本题所属考点:【弱电解质电离平衡】
本题难易程度:【一般】
Knowledge makes humble,ignorance makes proud. 知识使人谦虚,无知使人骄傲.
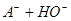
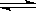
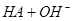 ,
,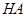
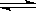
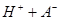 ;pH大于7,说明水解大于电离,所以[HA]>[A-] ,故A错误;[HA]一定大于0.05 mol・L-1 ,故B错误;根据物料守恒,2[Na+]="[HA]+[A-]" ,故C错误; 根据电荷守恒和物料守恒,2[OH-]=2[H+]+[HA]-[A-],故D正确。
;pH大于7,说明水解大于电离,所以[HA]>[A-] ,故A错误;[HA]一定大于0.05 mol・L-1 ,故B错误;根据物料守恒,2[Na+]="[HA]+[A-]" ,故C错误; 根据电荷守恒和物料守恒,2[OH-]=2[H+]+[HA]-[A-],故D正确。