微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 T1温度下,反应2SO2(g)+O2(g)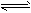 2SO3(g) △H<0的平衡常数K=532.4。
2SO3(g) △H<0的平衡常数K=532.4。
(1)该反应平衡常数的表达式为K= ,T1温度下,某时刻测得体系中各物质浓度分别为c(SO2)="0.0600" mol・L-1,c(O2)="0.400" mol・L-1,c(SO3)=2.000mol・L-1,此时反应进行的方向为 。
(2)该反应△S 0,升高温度,平衡常数 (填“增大”“减小”或“不变”)
(3)T2温度下,2L容积固定的甲、乙两密闭容器中发生上述反应,测得平衡时有关数据如下:
容器
| 甲
| 乙
|
反应物投入量
| 2molSO2、1molO2
| 4molSO3
|
平衡时n(SO3)/mol
| 1
| m
|
反应物的转化率
| ?1
| ?2
|
①下列能说明T2温度下甲容器中上述反应已达到平衡状态的是 。
A.SO2、O2、SO3的物质的量浓度之比为2:1:2
B.容器内气体压强不再变化
C.单位时间内2v(SO2)消耗= v(O2)生成
D.容器内混合气体的密度不再变化
②分析表格中数据,?1+?2 1(填“>”“=”或“<”),T1 T2(填“>”“=”或“<”)。
填空题 T1温 度下,反应2SO2(g)+O2(g)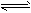 2SO3(g) △H<0的平衡常数K=532.4。
2SO3(g) △H<0的平衡常数K=532.4。
(1)该反应平衡常数的表达式为K= ,T1温度下,某时刻测得体系中各物质浓度分别为c(SO2)="0.0600" mol・L-1,c(O2)="0.400" mol・L-1,c(SO3)=2.000mol・L-1,此时反应进行的方向为 。
(2)该反应△S 0,升高温度,平衡常数 (填“增大”“减小”或“不变”)
(3)T2温度下,2L容积固定的甲、乙两密闭容器中发生上述反应,测得平衡时有关数据如下:
容器
| 甲
| 乙
|
反应物投入量
| 2molSO2、1molO2
| 4molSO3
|
平衡时n(SO3)/mol
| 1
| m
|
反应物的转化率
| ?1
| ?2
|
①下列能说明T2温度下甲容器中上述反应已达到平衡状态的是 。
A.SO2、O2、SO3的物质的量浓度之比为2:1:2
B.容器内气体压强不再变化
C.单位时间内2v(SO2)消耗= v(O2)生成
D.容器内混合气体的密度不再变化
②分析表格中数据,?1+?2 1(填“>”“=”或“<”),T1 T2(填“>”“=”或“<”)。
本题答案:(12分)(1)c2(SO3)/c2(SO2)c(O2),逆
本题解析:
试题分析:(1)c2(SO3)/c2(SO2)c(O2)= 2.0002/(0.06002×0.400)=2778>532.4,平衡向逆反应方向移动;(2)反应是一个体积减小的反应,该反应△S<0;△H<0,升高温度,平衡向逆反应方向移动,平衡常数减小;(3)①A、SO2、O2、SO3的物质的量浓度不再变化,物质的量浓度之比为2:1:2,达到平衡状态;B、反应是一个体积减小的反应,容器内气体压强不再变化,达到平衡状态;C、单位时间内2v(SO2)消耗= v(O2)生成 ,正逆反应速不相等,没有达到平衡状态;D、密闭容器中,质量守恒,密度不变,不能说明达到平衡状态;答案选AB。②若在容器乙中投入2mol SO3 ,?1+?2=1,投入4molSO3 ,压强增大,平衡右移?2减小,?1+?2<1;T2时平衡常数为12/(12×0.5)=2小于532.4,所以T1<T2。
考点:化学平衡常数
本题所属考点:【化学反应进行的方向】
本题难易程度:【一般】
Knowledge comes form diligence. 知识源于勤奋.