微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 在80℃时,将0.4mol的A气体充入2L已抽空的固定容积的密闭容器中发生反应:A(g) mB(g)隔一段时间对该容器内的物质进行分析,得到如下数据:
mB(g)隔一段时间对该容器内的物质进行分析,得到如下数据:
时间(s)
c(mol/L)
| 0
| 20
| 40
| 60
| 80
| 100
|
c(A)
| 0.20
| 0.14
| 0.10
| c
| d
| e
|
c(B)
| 0.00
| 0.12
| b
| 0.22
| 0.22
| 0.22
|
⑴m= ,表中b c(填“<”、“=”或“>”)。
⑵100秒后若将容器的体积缩小至原来一半,平衡时B的浓度____________0.44 mol/L(填“<”、“=”或“>”)。
⑶在80℃时该反应的平衡常数K值为 (保留1位小数)。
⑷在其他条件相同时,该反应的K值越大,表明建立平衡时 。
①A的转化率越高 ②B的产量越大
③A与B的浓度之比越大 ④正反应进行的程度越大
填空题 在80℃时,将0.4mol的A气体充入2L已抽空的固定容积的密闭容器中发生反应:A(g) mB(g)隔一段时间对该容器内的物质进行分析,得到如下数据:
mB(g)隔一段时间对该容器内的物质进行分析,得到如下数据:
时间(s)
c(mol/L)
| 0
| 20
| 40
| 60
| 80
| 100
|
c(A)
| 0.20
| 0.14
| 0.10
| c
| d
| e
|
c(B)
| 0.00
| 0.12
| b
| 0.22
| 0.22
| 0.22
|
⑴m= ,表中b c(填“<”、“=” 91ExAM.org或“>”)。
⑵100秒后若将容器的体积缩小至原来一半,平衡时B的浓度____________0.44 mol/L(填“<”、“=”或“>”)。
⑶在80℃时该反应的平衡常数K值为 (保留1位小数)。
⑷在其他条件相同时,该反应的K值越大,表明建立平衡时 。
①A的转化率越高 ②B的产量越大
③A与B的浓度之比越大 ④正反应进行的程度越大
本题答案:⑴2,> ⑵< ⑶0.5,
本题解析:
试题分析:(1)反应进行到20s时,A、B的浓度变化量分别是0.06mol/L、0.12mol/L,所以m=2;则根据方程式可知2×(0.10-c)=0.22-b,解得b-2c=0.02,所以b大于c。
100秒后若将容器的体积缩小至原来一半,瞬间B的浓度是0.44mol/L,但平衡向逆反应方向移动,所以平衡时B的浓度小于0.44mol/L。
(3)根据表中数据可知,反应进行到60s时物质的浓度不再发生变化,则反应达到平衡状态,生成B的浓度是0.22mol/L,则A的浓度应该是0.20mol/L-0.11mol/L=0.09mol/L,所以平衡常数K=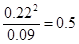
(4)化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,据此可知,如果该反应的K值越大,表明建立平衡时A的转化率越高、B的产量越大、正反应进行的程度越大,但A与B的浓度之比越大越小,答案选①③④。
考点:考查外界条件对平衡状态的影响以及平衡常数的有关计算和应用
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生能力的培养和解题方法的指导与训练,有利于培养学生的逻辑推理能力和抽象思维能力,提高学生灵活运用基础知识解决实际问题的能力。
本题所属考点:【化学平衡】
本题难易程度:【一般】
Wisdom is better than gold or silver. 知识胜过金银.