微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 氨基甲酸铵常用于生产医药试剂、发酵促进剂、电子元件等,是一种可贵的氨化剂。某学习小组研究在实验室中制备氨基甲酸铵的化学原理。
(1)将体积比为2:1的NH3和CO2混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生反应并达到平衡:2NH3(g)+CO2(g)  NH2COONH4(s)
NH2COONH4(s)
将实验测得的不同温度下的平衡数据列于下表:
温度(℃)
| 15.0
| 20.0
| 25.0
| 30.0
| 35.0
|
平衡总压强(kPa)
| 5.7
| 8.3
| 12.0
| 17.1
| 24.0
|
平衡气体总浓度 (10-3mol/L)
| 2.4
| 3.4
| 4.8
| 6.8
| 9.4
|
①上述反应的的焓变:?H 0,熵变?S 0(填“>”、“<”或“=”)
根据表中数据,计算出25.0℃时2NH3(g)+CO2(g)  NH2COONH4(s)的化学平衡常数K= 。
NH2COONH4(s)的化学平衡常数K= 。
③若从已达平衡状态的上述容器中分离出少量的氨基甲酸铵晶体,反应物的转化率将 (填“增大”、“减小”或“不变”)。
(2)氨基甲酸铵极易水解:NH2COONH4+2H2O  NH4HCO3+NH3・H2O。该学习小组为亲身体验其水解反应,分别取两份制得的样品,将其溶于水中并配制成不同浓度的氨基甲酸铵溶液,绘制出c(NH2COO―)随时间(t)变化的曲线如图所示,若A、B分别为不同温度时测定的曲线,则 (填“A”或“B”)曲线所对应的实验温度高,判断的依据是 。
NH4HCO3+NH3・H2O。该学习小组为亲身体验其水解反应,分别取两份制得的样品,将其溶于水中并配制成不同浓度的氨基甲酸铵溶液,绘制出c(NH2COO―)随时间(t)变化的曲线如图所示,若A、B分别为不同温度时测定的曲线,则 (填“A”或“B”)曲线所对应的实验温度高,判断的依据是 。

填空题 氨基甲酸铵常用于生产医药试剂、发酵促进剂、电子元件等,是一种可贵的氨化剂。某学习小组研究在实验室中制备氨基甲酸铵的化学原理。
(1)将体积比为2:1的NH3和CO2混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生反应并达到平衡:2NH3(g)+CO2(g)  NH2COONH4(s)
NH2COONH4(s)
将实验测得的不同温度下的平衡数据列于下表:
温度(℃)
| 15.0
| 20.0
| 25.0
| 30.0
| 35.0
|
平衡总压强(kPa)
| 5.7
| 8.3
| 12.0
| 17.1
| 24.0
|
平衡气体总浓度 (10-3mol/L)
| 2.4
| 3.4
| 4.8
| 6.8
| 9.4
|
①上述反应的的焓变:?H 0,熵变?S 0(填“>”、“<”或“=”)
根据表中数据,计算出25.0℃时2NH3(g)+CO2(g)  NH2COONH4(s)的化学平衡常数K = 。
NH2COONH4(s)的化学平衡常数K = 。
③若从已达平衡状态的上述容器中分离出少量的氨基甲酸铵晶体,反应物的转化率将 (填“增大”、“减小”或“不变”)。
(2)氨基甲酸铵极易水解:NH2COONH4+2H2O  NH4HCO3+NH3・H2O。该学习小组为亲身体验其水解反应,分别取两份制得的样品,将其溶于水中并配制成不同浓度的氨基甲酸铵溶液,绘制出c(NH2COO―)随时间(t)变化的曲线如图所示,若A、B分别为不同温度时测定的曲线,则 (填“A”或“B”)曲线所对应的实验温度高,判断的依据是 。
NH4HCO3+NH3・H2O。该学习小组为亲身体验其水解反应,分别取两份制得的样品,将其溶于水中并配制成不同浓度的氨基甲酸铵溶液,绘制出c(NH2COO―)随时间(t)变化的曲线如图所示,若A、B分别为不同温度时测定的曲线,则 (填“A”或“B”)曲线所对应的实验温度高,判断的依据是 。

本题答案:(1)①<,<(各2分,共4分)
②K=6.10×10
本题解析:
试题分析:(1)①从表中数据可以看出,随着温度升高,气体的总浓度增大,平衡正向移动,则该反应为吸热反应,△H>0;反应中固体变为气体,混乱度增大,△S>0;
②容器内气体的浓度之比为2:1,故NH3和CO2的浓度分别为3.2×10-3 mol・L-1、1.6×10-3 mol・L-1,代入平衡常数表达式:K=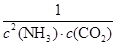 =
=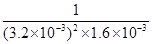 =6.10×107(L・mol-1)3;
=6.10×107(L・mol-1)3;
③若从已达平衡状态的上述容器中分离出少量的氨基甲酸铵晶体,氨基甲酸铵是固体,取出少量,化学平衡不移动,反应物的转化率将不变(2分)
(2) A 曲线所对应的实验温度高, A曲线起始浓度小,但在20min时间内反应速率快,说明其温度高。
考点:考查化学平衡。
本题所属考点:【化学平衡】
本题难易程度:【困难】
Wisdom is more precious than wealth. 智慧比财富更宝贵.