|
|
|
2013年12月15日4时搭载长征系列火箭的“玉兔号”顺利驶抵月球表?【化学平衡】
2016-12-26 15:36:57
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 2013年12月15日4时搭载长征系列火箭的“玉兔号”顺利驶抵月球表面,实现了五星红旗耀月球的创举。火箭升空需要高能燃料,通常用肼(N2H4)作燃料,N2O4做氧化剂。请回答下列问题:
(1)已知:N2(g) + 2O2(g) ="=" 2NO2(g) ΔH= + 67.7kJ・mol-1
N2H4(g) + O2(g)="=" N2(g) + 2H2O(g) ΔH= - 534.0kJ・mol-1
2NO2(g) 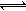 N2O4(g) ΔH=" -" 52.7kJ・mol-1 N2O4(g) ΔH=" -" 52.7kJ・mol-1
写出气态肼在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式: ;
(2)工业上用次氯酸钠与过量的氨气反应制备肼,该反应的化学方程式为: ;
(3)工业上可以用下列反应原理制备氨气:
2N2(g)+6H2O(l)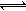 4NH3(g)+3O2(g) ΔH= Q kJ・mol-1 4NH3(g)+3O2(g) ΔH= Q kJ・mol-1
①已知该反应的平衡常数K与温度的关系如图,则此反应的 Q 0 (填“>”“<”或“=”)。

②若起始加入氮气和水,15分钟后,反应达到平衡,此时NH3的浓度为0.3mol/L,则用氧气表示的反应速率为 。
③常温下,如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时, (选填编号).
A.容器中气体的平均相对分子质量不随时间而变化
B.v(N2)/v(O2)=2∶3
C.容器中气体的密度不随时间而变化
D.通入稀有气体能提高反应的速率
| E.若向容器中继续加入N2,N2的转化率将增大
(4)最近华南理工大提出利用电解法制H2O2并以此处理废氨水,装置如图。
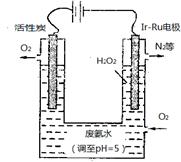
①为不影响H2O2的产量,需要向废氨水加入适量硝酸调节溶液的pH约为5,则所得废氨水溶液中c(NH4+) c(NO3-)(填“>”“<”或“=”);
②Ir―Ru惰性电极有吸附O2作用,该电极的电极反应为 ;
③理论上电路中每转移3mol电子,最多可以处理NH3・H2O的物质的量为 。
填空题 2013年12月15日4时搭载长征系列火箭的“玉兔号”顺利驶抵月球表面,实现了五星红旗耀月球的创举。火箭升空需要高能燃料,通常用肼(N2H4)作燃料,N2O4做氧化剂。请回答下列问题:
(1)已知:N2(g) + 2O2(g) ="=" 2NO2(g) ΔH= + 67.7kJ・mol-1
N2H4(g) + O2(g)="=" N2(g) + 2H2O(g) ΔH= - 534.0kJ・mol-1
2NO2(g) 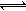 N2O4(g) ΔH=" -" 52.7kJ・mol-1 N2O4(g) ΔH=" -" 52.7kJ・mol-1
写出气态肼在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式: ;
(2)工业上用次氯酸钠与过量的氨气反应制备肼, 该反应的化学方程式为: ;
(3)工业上可以用下列反应原理制备氨气:
2N2(g)+6H2O(l)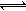 4NH3(g)+3O2(g) ΔH= Q kJ・mol-1 4NH3(g)+3O2(g) ΔH= Q kJ・mol-1
①已知该反应的平衡常数K与温度的关系如图,则此反应的 Q 0 (填“>”“<”或“=”)。

②若起始加入氮气和水,15分钟后,反应达到平衡,此时NH3的浓度为0.3mol/L,则用氧气表示的反应速率为 。
③常温下,如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时, (选填编号).
A.容器中气体的平均相对分子质量不随时间而变化
B.v(N2)/v(O2)=2∶3
C.容器中气体的密度不随时间而变化
D.通入稀有气体能提高反应的速率
|
E.若向容器中继续加入N2,N2的转化率将增大
(4)最近华南理工大提出利用电解法制H2O2并以此处理废氨水,装置如图。

①为不影响H2O2的产量,需要向废氨水加入适量硝酸调节溶液的pH约为5,则所得废氨水溶液中c(NH4+)
c(NO3-)(填“>”“<”或“=”);
②Ir―Ru惰性电极有吸附O2作用,该电极的电极反应为
;
③理论上电路中每转移3mol电子,最多可以处理NH3・H2O的物质的量为
。
本题答案:(1)2N2H4(g) + N2O4(g)=3N2(g) +
本题解析:
本题所属考点:【化学平衡】
本题难易程度:【困难】
There is no mistake so great as that of being always right. 最大的错误莫过于总是自信正确。

