|
|
|
温度为T时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g【化学平衡】
2016-12-26 15:38:21
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 温度为T时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g) PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据如图: PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据如图:
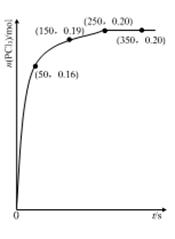
下列说法正确的是
A.反应在前50 s 的平均速率v(PCl3)=0.0032 mol・L-1・s-1
B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol・L-1,则反应的△H<0
C.相同温度下,起始时向容器中充入2.0 mol PCl3和2.0mol Cl2,达到平衡时,PCl3的转化率小于80%
D.相同温度下 ,起始时向容器中充入1.0 mol PCl5、0.20mol PCl3和0.20 mol Cl2,反应达到平衡前v(正)>v(逆)
|
填空题 温度为T时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g) PCl3(g)+Cl2(g)经过一段时间 后达到平衡。反应过程中测定的部分数据如图: PCl3(g)+Cl2(g)经过一段时间 后达到平衡。反应过程中测定的部分数据如图:

下列说法正确的是
A.反应在前50 s 的平均速率v(PCl3)=0.0032 mol・L-1・s-1
B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol・L-1,则反应的△H<0
C.相同温度下,起始时向容器中充入2.0 mol PCl3和2.0mol Cl2,达到平衡时,PCl3的转化率小于80%
D.相同温度下,起始时向容器中充入1.0 mol PCl5、0.20mol PCl3和0.20 mol Cl2,反应达到平衡前v(正)>v(逆)
|
本题答案:D
本题解析:
试题分析:A、反应在前50 s 的平均速率v(PCl3)=0.16÷2÷50="0.0016" mol・L-1・s-1,错误;B、平衡时c(PCl3)=0.20÷2=0.10mol・L-1,升高温度其浓度增大,平衡正向移动,反应吸热,错误;C、相同温度下,起始时向容器中充入1.0 mol PCl3和1.0 mol Cl2时与元平衡为等效平衡, PCl3的转化率小于80% ,充入2.0 mol PCl3和2.0 mol Cl2,压强增大平衡向生成PCl5方向移动,PCl3的转化率增大,错误;
PCl5(g)

PCl3(g)+Cl2(g)
始量 1 0 0
转化量 0.2 0.2 0.2
平衡量 0.8 0.2 0.2
k=(0.2/2×0.2/2)÷0.8/2=0.025
此时浓度熵Q=(0.2/2×0.2/2)÷1.0/2=0.02<0.025,平衡正向移动,v(正)>v(逆),正确。
考点:考查化学平衡有关问题。
本题所属考点:【化学平衡】
本题难易程度:【一般】
He that is a master must serve. 一家之主必为全家操劳.
 PCl3(g)+Cl2(g)
PCl3(g)+Cl2(g)