|
|
|
(16分)已知2SO2(g)十O2(g)<img src="http://www.91exam.or【化学平衡】
2016-12-26 15:45:07
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (16分)已知2SO2(g)十O2(g)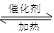 2SO3(g)反应过程的 能量变化如图所示。 2SO3(g)反应过程的 能量变化如图所示。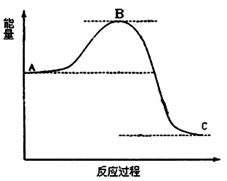
请回答下列问题:
(1)1mol SO2(g)氧化为1mol SO3(g)放出的热量为99.00kJ・mol-1,写出该反应的热化学方程式 。
(2)①在图中标出该反应的活化能E和反应热△H;
②该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低,请在图中画图表示出来,并进行必要的标注。
(3)能够说明在恒温恒容条件下,上述反应已经达到化学平衡状态的是 。
| A.容器中气体总压强不变 | B.容器中混合气体的密度不变
| | C.每生成1mol SO3的同时生成1molSO2 | D.SO2、O2、SO3的物质的量之比为2∶1∶2
| (4)在400℃,常压下,向体积为2L的密闭容器中充入2mol SO2(g)和1.92mol O2(g),充分反应后,测得还有0.08mol SO2剩余,求该反应的平衡常数(要求写出计算过程)。
填空题 (16分)已知2SO2(g)十O2(g)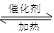 2SO3(g)反应过程的能量变化如图所示。 2SO3(g)反应过程的能量变化如图所示。
请回答下列问题:
(1)1mol SO2(g)氧化为1mol SO3(g)放出的热量为99.00kJ・mol-1,写出该反应的热化学方程式 。
(2)①在图中标出该反应的活化能E和反应热△H;
②该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低,请在图中画图表示出来,并进行必要的标注。
(3)能够说明在恒温恒容条件下,上述反应已经达到化学平衡状态的是 。
| A.容器中气体总压强不变 | B.容器中混合气体的密度不变
|
| C.每生成1mol SO3的同时生成1molSO2 | D.SO2、O2、SO3的物质的量之比为2∶1∶2
|
(4)在400℃,常压下,向体积为2L的密闭容器中充入2mol SO2(g)和1.92mol O2(g),充分反应后,测得还有0.08mol SO2剩余,求该反应的平衡常数(要求写出计算过程)。
本题答案:(1)2SO2(g)十O2(g)
1mol SO2(g)氧化为1mol SO3(g)放出的热量为99.00kJ・mol-1,则该反应的热化学方程式是2SO2(g)十O2(g)<img onload='if(this.width>600)makesmallpic(this,600,1800);' src=)
2SO3(g) △H=-198.00 kJ/mo1;(2)①在图中标出该反应的活化能E和反应热△H如图:

;②该反应通常用V2O5作催化剂,加V2O5会使图中B点降低,在图中画图表示出来,并进行必要的标注。(3)A.由于该反应是在恒温恒容的密闭容器内进行的。反应是气体体积减小的反应,所以若容器中气体总压强不变,则反应达到平衡,正确;B.反应前后气体的质量不变,容器的容积不变,所以无论反应是否达到平衡,容器中混合气体的密度都不变,因此不能作为判断平衡的标志,错误;C每生成1mol SO3就会消耗1mol的SO2,同时生成1molSO2,则SO2的物质的量浓度不变,反应达到平衡,正确;D.SO2、O2、SO3的物质的量之比为2∶1∶2是非常特殊的情况,这与加入的物质的多少有关,反应可能处于平衡状态,也可能未达到平衡,不能作为判断平衡的标志,错误。(4) 2SO2(g) 十 O2(g)

2SO3(g)
C始(mol/L) 2mol/2L ="1mol/L" 1.92mol/2L=0.96mol/L 0
△C(mol/L) 0.96mol/L 0.48 0.96
C平(mol/L) 0.08mol/2L =0.04 0.48 0.96
K= C2(SO3)/C2(SO2) C(O2) = (0.96mol/L)2/(0.04mol/L)2×0.48mol/L =" 1200" L/mol
考点:考查热化学方程式的书写、反应热、活化能、反应速率的影响因素、可逆反应平衡状态的判断、化学平衡常数的计算的知识。
本题所属考点:【化学平衡】
本题难易程度:【一般】
One loses time seeking for words; one kiss brings understanding. 寻找言辞徒费时光,一吻即可得理解.
 ;②该反应通常用V2O5作催化剂,加V2O5会使图中B点降低,在图中画图表示出来,并进行必要的标注。(3)A.由于该反应是在恒温恒容的密闭容器内进行的。反应是气体体积减小的反应,所以若容器中气体总压强不变,则反应达到平衡,正确;B.反应前后气体的质量不变,容器的容积不变,所以无论反应是否达到平衡,容器中混合气体的密度都不变,因此不能作为判断平衡的标志,错误;C每生成1mol SO3就会消耗1mol的SO2,同时生成1molSO2,则SO2的物质的量浓度不变,反应达到平衡,正确;D.SO2、O2、SO3的物质的量之比为2∶1∶2是非常特殊的情况,这与加入的物质的多少有关,反应可能处于平衡状态,也可能未达到平衡,不能作为判断平衡的标志,错误。(4) 2SO2(g) 十 O2(g)
;②该反应通常用V2O5作催化剂,加V2O5会使图中B点降低,在图中画图表示出来,并进行必要的标注。(3)A.由于该反应是在恒温恒容的密闭容器内进行的。反应是气体体积减小的反应,所以若容器中气体总压强不变,则反应达到平衡,正确;B.反应前后气体的质量不变,容器的容积不变,所以无论反应是否达到平衡,容器中混合气体的密度都不变,因此不能作为判断平衡的标志,错误;C每生成1mol SO3就会消耗1mol的SO2,同时生成1molSO2,则SO2的物质的量浓度不变,反应达到平衡,正确;D.SO2、O2、SO3的物质的量之比为2∶1∶2是非常特殊的情况,这与加入的物质的多少有关,反应可能处于平衡状态,也可能未达到平衡,不能作为判断平衡的标志,错误。(4) 2SO2(g) 十 O2(g) 2SO3(g)
2SO3(g)