|
|
|
下图为装有活塞(质量忽略不计)的密闭容器,内盛22.4mL一氧化?【化学平衡】
2016-12-26 15:59:26
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 下图为装有活塞(质量忽略不计)的密闭容器,内盛22.4mL一氧化氮,若通入11.2mL氧气(气体体积均在标准状况下测定),保持温度压强不变,则容器内的密度为(提示:不考虑NO转化为NO2的可逆性)

A.等于1.369 g・L-1
B.等于2.054 g・L-1
C.在1.369g・L-1和2.054g・L-1之间
D.在2.054g・L-1和4.108g・L-1之间
|
选择题 下图为装有活塞(质量忽略不计)的密闭容器,内盛22.4mL一氧化氮,若通入11.2mL氧气(气体体积均在标准状况下测定),保持温度压强不变,则容器内的密度为(提示:不考虑NO转化为NO2的可逆性)

A.等于1.369 g・L-1
B.等于2.054 g・L-1
C.在1.369g・L-1和2.054g・L-1之间
D.在2.054g・L-1和4.108g・L-1之间
|
本题答案:D
本题解析:
试题分析:NO与氧气恰好符合物质的量之比 是2:1的关系,所以二者恰好完全反应生成NO2,若全部是二氧化氮,则恒压下气体的密度即为二氧化氮在标准状况下的密度46g/22.4L=2.054g/L,但二氧化氮存在
如下平衡2NO2
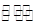
N2O4 ,若二氧化氮全部转化为N2O4,恒压下气体的密度是N2O4的密度为92g/22.4L=4.108g/L,而实际的气体的密度应介于二者之间,所以答案选D。
考点:考查混合气体密度的判断,极端假设法的应用
本题所属考点:【化学平衡】
本题难易程度:【一般】
A good beginning makes a good ending. 欲善其终,先善其始.
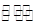 N2O4 ,若二氧化氮全部转化为N2O4,恒压下气体的密度是N2O4的密度为92g/22.4L=4.108g/L,而实际的气体的密度应介于二者之间,所以答案选D。
N2O4 ,若二氧化氮全部转化为N2O4,恒压下气体的密度是N2O4的密度为92g/22.4L=4.108g/L,而实际的气体的密度应介于二者之间,所以答案选D。