|
|
|
80℃时,2L密闭容器中充入0.40molN2O4,发生反应N2O4<img src【化学平衡】
2016-12-26 16:01:09
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 80℃时,2L密闭容器中充入0.40molN2O4,发生反应
N2O4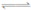 2NO2 2NO2 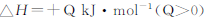 ,获得如下数据: ,获得如下数据:
 下列判断正确的是 下列判断正确的是
A.升高温度该反应的平衡常数K减小
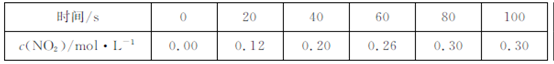
B.20~40s内,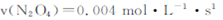
C.反应达平衡时,吸收的热量为0.30QkJ
D.100s时再通入0.40molN2O4,达新平衡时N2O4的转化率增大
|
选择题 80℃时,2L密闭容器中充入0.40molN2O4,发生反应
N2O4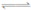 2NO2 2NO2 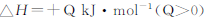 ,获得如 下数据: ,获得如 下数据:
 下列判断正确的是 下列判断正确的是
A.升高温度该反应的平衡常数K减小
B.20~40s内,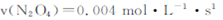
C.反应达平衡时,吸收的热量为0.30QkJ
D.100s时再通入0.40molN2O4,达新平衡时N2O4的转化率增大
|
本题答案:C
本题解析:
试题分析: A?该反应为吸热反应,温度升高,平衡向吸热的方向移动,即正反应方向移动,平衡常数K增大,故A错误;B?20~40s 内
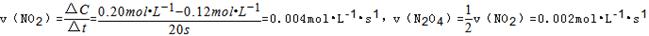
C?浓度不变时,说明反应已达平衡,反应达平衡时,生成NO2的物质的量为0.30mol?L-1×2L=0.60mol,由热化学方程式可知生成2molNO2吸收热量QkJ,所以生成0.6molNO2吸收热量0.3QkJ,故C正确;D?100s时再通入0.40mol N2O4,平衡状态相当于增大压强,平衡逆向移动,N2O4的转化率减小,故D错误;故选C.
考点:考查化学反应速率?化学平衡移动以及热量的有关计算
本题所属考点:【化学平衡】
本题难易程度:【一般】
No mill, no meal. 不磨面,没饭吃.
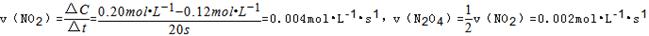 C?浓度不变时,说明反应已达平衡,反应达平衡时,生成NO2的物质的量为0.30mol?L-1×2L=0.60mol,由热化学方程式可知生成2molNO2吸收热量QkJ,所以生成0.6molNO2吸收热量0.3QkJ,故C正确;D?100s时再通入0.40mol N2O4,平衡状态相当于增大压强,平衡逆向移动,N2O4的转化率减小,故D错误;故选C.
C?浓度不变时,说明反应已达平衡,反应达平衡时,生成NO2的物质的量为0.30mol?L-1×2L=0.60mol,由热化学方程式可知生成2molNO2吸收热量QkJ,所以生成0.6molNO2吸收热量0.3QkJ,故C正确;D?100s时再通入0.40mol N2O4,平衡状态相当于增大压强,平衡逆向移动,N2O4的转化率减小,故D错误;故选C.