|
(16分).联氨(N2H4)及其衍生物是一类重要的火箭燃料。N2H4与N【化学平衡】
(3) 17℃、1.01×105Pa,往10L密闭容器中充入NO2,达到平衡时,c(NO2)="0.2" mol・L-1, c(N2O4)="0.16" mol・L-1。则反应初始时,充入NO2的物质的量为 ;NO2的转化率为 ;该温度下该反应的平衡常数K为 ;该温度下反应N2O4(g)  2NO2(g)的平衡常数K为 。 2NO2(g)的平衡常数K为 。 填空题 (16分).联氨(N2H4)及其衍生物是一类重要的火箭燃料。N2H4与N2O4反应能放出大量的热。(1)已知:2NO2(g) |
 2NO2(g)的平衡常数K为 。
2NO2(g)的平衡常数K为 。 N2O4(g)是熵减的反应,若反应能够自发进行,则焓减即反应的ΔH<0;
N2O4(g)是熵减的反应,若反应能够自发进行,则焓减即反应的ΔH<0;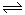 2NO2(g)的平衡常数K为1/4.
2NO2(g)的平衡常数K为1/4.本题所属考点:【化学平衡】
本题难易程度:【一般】
|
||
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | ||
| 下一篇:(10分)两种气态单质X和Y能直接化.. | ||