|
|
|
将0.20 mol NO和0.1 mol CO充入一个容积恒定为1L的密闭容中发生?【化学平衡】
2016-12-26 16:17:45
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 ; 将0.20 mol NO和0.1 mol CO充入一个容积恒定为1L的密闭容中发生反应:2NO(g)+2CO(g) N2(g)+2CO2(g) △H<0在不同条件下,反应过程中部分物质的浓度变化如图所示。 N2(g)+2CO2(g) △H<0在不同条件下,反应过程中部分物质的浓度变化如图所示。
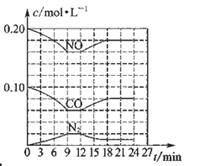
下列说法正确的是
A.容器内的压强不发生变化说明该反应达到平衡
B.当向容器中再充入0.20 mol NO时,平衡向正反应方向移动,K增大
C.第12 min时改变的反应条件为升高温度
D.向该容器内充入He气,容器内气体压强增大,所以反应速率增大
|
选择题 将0.20 mol NO和0.1 mol CO充入一个容积恒定为1L的密闭容中发生反应:2NO(g)+2CO(g) N2(g)+2CO2(g) △H<0在不同条件下,反应过程中部分物质的浓度变化如图所示。 N2(g)+2CO2(g) △H<0在不同条件下,反应过程中部分物质的浓度变化如图所示。

下列说法正确的是
A.容器内的压强不发生变化说明该反应达到平衡
B.当向容器中再充入0.20 mol NO时,平衡向正反 应方向移动,K增大
C.第12 min时改变的反应条件为升高温度
D.向该容器内充入He气,容器内气体压强增大,所以反应速率增大
|
本题答案:A
本题解析:
试题分析:A、根据方程式可知,正方应是体积减小的可逆反应,因此当压强不再发生变化时,可以说明反应达到平衡状态,A正确;B、平衡常数只与温度有关系,因此当温度不变时平衡常数不变,B错误;C、根据图像可知,第12min时反应物的浓度逐渐升高,而生成物的浓度逐渐降低,这说明平衡向逆反应方向移动,由于正方应是放热、体积减小的反应,所以改变的条件是升高温度或降低压强或增大CO2的浓度,C错误;D、容器容积不变,充入He气,压强增大,但反应物的浓度不变,反应速率不变,D错误,答案选A。
考点:考查平衡状态判断以及外界条件对反应速率和平衡状态的影响
本题所属考点:【化学平衡】
本题难易程度:【困难】
First think, then speak. 熟思而后言.