微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 2SO2(g)+O2(g)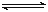 2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙、丁四个容器体积均为2 L的恒容密闭容器中投料,其起始物质的量及含硫反应物的平衡转化率如下表所示:
2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙、丁四个容器体积均为2 L的恒容密闭容器中投料,其起始物质的量及含硫反应物的平衡转化率如下表所示:
|
| 甲
| 乙
| 丙
| 丁
|
起始物质的量
| n(SO2)/mol
| 0.40
| 0
| 0.80
| 0.02
|
n(O2)/mol
| 0.24
| 0
| 0.48
| 0.04
|
n(SO3)/mol
| 0
| 0.40
| 0
| 0.40
|
含硫反应物的平衡转化率%
| 80
| 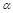 1 1
| 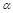 2 2
| 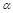 3 3
|
下列判断中,正确的是
A.乙中SO3的平衡转化率为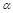 1=20%
1=20%
B.平衡时,丙中c(SO3)是甲中的2倍
C.平衡时,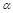 3<
3<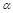 1
1
D.该温度下,平衡常数的值为400
选择题 2SO2(g)+O2(g)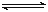 2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙、丁四个容器体积均为2 L的恒容密闭容器中投料,其起始物质的量及含硫反应 物的平衡转化率如下表所示:
2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙、丁四个容器体积均为2 L的恒容密闭容器中投料,其起始物质的量及含硫反应 物的平衡转化率如下表所示:
|
| 甲
| 乙
| 丙
| 丁
|
起始物质的量
| n(SO2)/mol
| 0.40
| 0
| 0.80
| 0.02
|
n(O2)/mol
| 0.24
| 0
| 0.48
| 0.04
|
n(SO3)/mol
| 0
| 0.40
| 0
| 0.40
|
含硫反应物的平衡转化率%
| 80
| 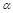 1 1
| 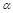 2 2
| 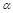 3 3
|
下列判断中,正确的是
A.乙中SO3的平衡转化率为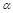 1=20%
1=20%
B.平衡时,丙中c(SO3)是甲中的2倍
C.平衡时,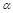 3<
3<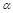 1
1
D.该温度下,平衡常数的值为400
本题答案:CD
本题解析:
试题分析:对于甲,由于SO2的转化率是80%,所以平衡时各种物质的物质的量分别是:n(SO2)=0.08mol;n(O2)=0.08mol;n(SO3)=0.32mol;所以在该温度下的化学平衡产生K=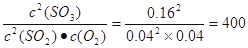 。温度不变,化学平衡常数就不变。A.由于反应是在恒温恒容条件下进行的,对于相当于开始加入n(SO2)=0.4mol;n(O2)=0.2mol;n(SO3)="0" mol。由于氧气的浓度比甲小,所以SO2的转化率小于80%,即SO3的转化率
。温度不变,化学平衡常数就不变。A.由于反应是在恒温恒容条件下进行的,对于相当于开始加入n(SO2)=0.4mol;n(O2)=0.2mol;n(SO3)="0" mol。由于氧气的浓度比甲小,所以SO2的转化率小于80%,即SO3的转化率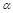 1>20%,错误;B.对于丙由于开始加入的二氧化硫和氧气的物质的量是甲的二倍,增大了反应物的浓度,平衡正向移动,SO2的转化率增大,。但是平衡移动的趋势是微弱的,所以平衡时丙中c(SO3)比甲中的2倍要小的多,错误;C.由于丁中开始加入的各种物质的物质的量分别是:n(SO2)=0.02mol;n(O2)=0.04mol;n(SO3)="0.4" mol,可以等效转化,认为SO3是反应产生的,则其等效开始状态是n(SO2)=0.42mol;n(O2)=0.24mol;n(SO3)="0" mol,氧气的浓度不变,而增大了SO2的浓度。增大反应物的浓度,能够使其它反应物的转化率提高,而其本身的转化率反而降低,所以平衡时,
1>20%,错误;B.对于丙由于开始加入的二氧化硫和氧气的物质的量是甲的二倍,增大了反应物的浓度,平衡正向移动,SO2的转化率增大,。但是平衡移动的趋势是微弱的,所以平衡时丙中c(SO3)比甲中的2倍要小的多,错误;C.由于丁中开始加入的各种物质的物质的量分别是:n(SO2)=0.02mol;n(O2)=0.04mol;n(SO3)="0.4" mol,可以等效转化,认为SO3是反应产生的,则其等效开始状态是n(SO2)=0.42mol;n(O2)=0.24mol;n(SO3)="0" mol,氧气的浓度不变,而增大了SO2的浓度。增大反应物的浓度,能够使其它反应物的转化率提高,而其本身的转化率反而降低,所以平衡时,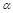 3<
3<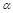 1,正确;D.根据选项A的计算可知该温度下,平衡常数的值为400,正确。
1,正确;D.根据选项A的计算可知该温度下,平衡常数的值为400,正确。
考点:考查物质的量浓度对化学平衡移动的影响、等效平衡、物质的转化率的比较和平衡产生的计算。
本题所属考点:【化学平衡】
本题难易程度:【困难】
In this world there is always danger for those who are afraid of it. 对于害怕危险的人,这个世界上总是有危险的。