|
|
|
(1)将一定量的N2(g)和H2(g)放入2L的密闭容器中,在500℃、2×1【化学平衡】
2016-12-26 16:43:09
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (1)将一定量的N2(g)和H2(g)放入2L的密闭容器中,在500℃、2×107Pa下发生如下反应:N2(g)+3H2(g) 2NH3(g) 2NH3(g)
①在反应体系中加入催化剂,反应速率 ,该反应的反应热 (填“增大”、“减小”或“不变”)。
②5分钟后达到平衡,测得N2为0.2 mol,H2为0.6 mol,NH3为0.2 mol。氮气的平均反应速率v(N2)= ,H2的转化率为 (保留小数点后一位)。
③欲提高②容器中H2的转化率,下列措施可行的是 。
| A.把气体的体积压缩至1L | B.向容器中再充入惰性气体
| | C.改变反应的催化剂 | D.液化生成物分离出氨
| (2)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3和TiO2)表面与水发生下列反应:
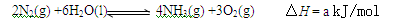
进一步研究NH3生成量与温度关系,常压下达到平衡时测得部分实验数据如下:
T/K
| 303
| 313
| 323
| NH3生成量/(10-6mol)
| 4.8
| 5.9 91eXaM.org
| 6.0
|
此合成反应的a 0。(填“大于”、“小于”或“等于”)
填空题 (1)将一定量的N2(g)和H2(g)放入2L的密闭容器中,在500℃、2×107Pa下发生如下反应:N2(g)+3H2(g) 2NH3(g) 2NH3(g)
①在反应体系中加入催化剂,反应速率 ,该反应的反应热 (填“增大”、“减小”或“不变”)。
②5分钟后达到平衡,测得N2为0.2 mol,H2为0.6 mol,NH3为0.2 mol。氮气的平均反应速率v(N2)= ,H2的转化率为 (保留小数点后一位)。
③欲提高②容器中H2的转化率,下列措施可行的是 。
| A.把气体的体积压缩至1 L | B.向容器中再充入惰性气体
|
| C.改变反应的催化剂 | D.液化生成物分离出氨
|
(2)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3和TiO2)表面与水发生下列反应:
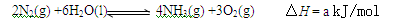
进一步研究NH3生成量与温度关系,常压下达到平衡时测得部分实验数据如下:
T/K
| 303
| 313
| 323
|
NH3生成量/(10-6mol)
| 4.8
| 5.9
| 6.0
|
此合成反应的a
0。(填“大于”、“小于”或“等于”)
本题答案:(1)①增大 不变 ②0.01mol・L-1・mi
本题解析:
试题分析:(1)①催化剂能增大化学反应速率,但不能改变反应热;②将一定量的N2(g)和H2(g)放入2L的密闭容器中,在500℃、2×107Pa下发生反应:N2(g)+3H2(g)?2NH3(g)5分钟后达到平衡,测得N2为0.2mol,H2为0.6mol,NH3为0.2mol.
依据化学平衡的三段式列式计算:起始量=平衡量+变化量
N2(g)+3H2(g)?2NH3(g)
起始量(mmol) 0.3 0.9 0
变化量(mol) 0.1 0.3 0.2
平衡量(mol) 0.2 0.6 0.2
氮气的平均反应速率v(N2)=
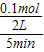
=0.01mol/L?min;
H2的转化率=

×100%=33.3%
③欲提高②容器中H2的转化率,A、增大压强,平衡向气体体积减小的方向进行移动,氢气转化率增大;B、加入惰性气体,相当于减少压强,平衡向气体体积增大的方向移动;C、催化剂不能改变反应物的转化率;D、减少生成物浓度,平衡向正反应方向移动;所以答案选AD
(2)升高温度,平衡向吸热反应方向移动即正反应方向移动,故a>0
考点:考查营销化学平衡移动以及转化率、化学反应速率的相关知识点。
本题所属考点:【化学平衡】
本题难易程度:【一般】
Never let your feet run faster than your shoes. 不要让你的脚跳得比你的鞋子快。
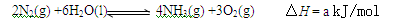
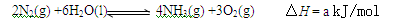
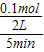 =0.01mol/L?min;
=0.01mol/L?min; ×100%=33.3%
×100%=33.3%