|
|
|
某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的【化学平衡】
2016-12-26 16:43:38
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量)
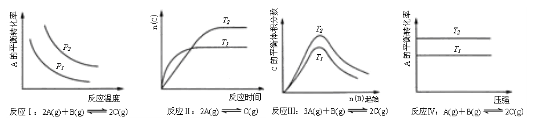
根据以上规律判断,上列结论正确的是
A.反应Ⅰ:△H>0,P2>P来源:91考试网 91ExAm.org1
B.反应Ⅱ:△H<0,T1>T2
C.反应Ⅳ:△H<0,T2>T1
D.反应Ⅲ:△H>0,T2>T1;或△H<0,T2<T1
|
选择题 某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量)

根据以上规律判断,上列结论正确的是
A.反应Ⅰ:△H>0,P2>P1
B.反应Ⅱ:△H<0,T1>T2
C.反应Ⅳ:△H<0,T2>T1
D.反应Ⅲ:△H>0,T2>T1;或△H<0,T2<T1
|
本题答案:B
本题解析:
试题分析:A.反应Ⅰ的特点是正反应方向为气体体积减小的方向,结合图像,压强增大,A的转化率应增大,所以p2>p1,随温度的升高A的转化率减小,所以正反应为放热反应,ΔH<0,A错误;B.关于反应Ⅱ,由图像可以看出,T1条件下达到平衡所用时间短,所以T1>T2,而在T1条件下达平衡时n(C)小,说明低温有利于C的生成,它的正反应为放热反应,ΔH<0,B正确;C,关于反应Ⅲ ,由图像可以看出,T2条件下C的平衡体积分数大,因此当T2>T1时正反应应为吸热反应,ΔH>0,而当T2<T1时,正反应应为放热反应,ΔH<0,C错误;D.关于反应Ⅳ,由图像可以看出,T2条件下A的转化率大,因此当T2>T1时,说明升高温度平衡向正反应方向移动,因此正反应为吸热反应,ΔH>0,D错误,选B。
考点:考查外界条件对平衡移动的影响。
本题所属考点:【化学平衡】
本题难易程度:【一般】
A baited cat may grow as fierce as a lion. 被逼急的猫,凶得象狮子。