微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 在300 mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:
Ni(s)+4CO(g)  Ni(CO)4(g),已知该反应平衡常数与温度的关系如下表,下列说法正确的是
Ni(CO)4(g),已知该反应平衡常数与温度的关系如下表,下列说法正确的是
温度/℃
| 25
| 80
| 230
|
平衡常数
| 5×104
| 2
| 1.9×10-5
|
A.上述生成Ni(CO)4的反应为吸热反应
B.25 ℃时,反应Ni(CO)4(g)  Ni(s)+4CO(g)的平衡常数为2×10-5
Ni(s)+4CO(g)的平衡常数为2×10-5
C.80 ℃达到平衡时,测得n(CO)=0.3 mol,则Ni(CO)4的平衡浓度为2 mol・L-1
D.80 ℃时,测得某时刻Ni(CO)4、CO的浓度均为0.5 mol・L-1,则此时 υ(正)>υ(逆)
选择题 在300 mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:
Ni(s)+4CO(g)  Ni(CO)4(g),已知该反应平衡常数与温度的关系如下表,下列说法正确的是
Ni(CO)4(g),已知该反应平衡常数与温度的关系如下表,下列说法正确的是
温度/℃
| 25
| 80
| 230
|
平衡常数
| 5×104
| 2
| 1.9×10-5
|
A.上述生成Ni(CO)4的反应为吸热反应
B.25 ℃时,反应Ni(CO)4(g)  Ni(s)+4CO(g)的平衡常数为2×10-5
Ni(s)+4CO(g)的平衡常数为2×10-5
C.80 ℃达到平衡时,测得n(CO)=0.3 mol,则Ni(CO)4的平衡浓度为 2 mol・L-1
D.80 ℃时,测得某时刻Ni(CO)4、CO的浓度均为0.5 mol・L-1,则此时υ(正)>υ(逆)
本题答案:BC
本题解析:
试题分析:A、根据表中数据可知,随着温度的升高,平衡常数逐渐减小。这说明升高温度平衡向逆反应方向移动,因此正反应是放热反应,A错误;B、逆反应的平衡常数是正反应平衡常数的倒数,则25℃时反应Ni(CO)4(g)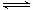 Ni(s)+4CO(g)的平衡常数为1/50000=2×10-5,B正确;C、80℃达到平衡时,n(CO)=0.3 mol,[ Ni(CO)4]/1=2,Ni(CO)4的平衡浓度为2 mol・L-1,C正确;D.在某条件下达到平衡,测得Ni(CO)4、CO浓度均为0.5mol/L,则此时0.5/0.54=8。由于正反应是放热反应,所以此时温度小于80℃,D错误;选BC。
Ni(s)+4CO(g)的平衡常数为1/50000=2×10-5,B正确;C、80℃达到平衡时,n(CO)=0.3 mol,[ Ni(CO)4]/1=2,Ni(CO)4的平衡浓度为2 mol・L-1,C正确;D.在某条件下达到平衡,测得Ni(CO)4、CO浓度均为0.5mol/L,则此时0.5/0.54=8。由于正反应是放热反应,所以此时温度小于80℃,D错误;选BC。
考点:考查平衡常数的判断和应用、外界条件对平衡状态的影响。
本题所属考点:【化学平衡】
本题难易程度:【一般】
Laziness in youth spells regret in old age. 少壮不努力,老大徒伤悲.