微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为 &# 160; 。利用反应6NO2+ 8NH3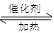 7N2+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L。
7N2+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L。
(2)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=?196.6 kJ・mol-1
2SO3(g) ΔH=?196.6 kJ・mol-1
2NO(g)+O2(g) 2NO2(g) ΔH =?113.0 kJ・mol-1
2NO2(g) ΔH =?113.0 kJ・mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH = kJ・mol-1。
SO3(g)+NO(g)的ΔH = kJ・mol-1。
一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO3的同时生成1 molNO2
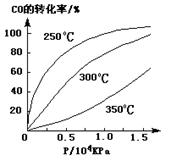
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。该反应ΔH 0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。该反应ΔH 0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
填空题 研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为 。利用反应6NO2+ 8NH3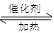 7N2+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L。
7N2+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L。
(2)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=?196.6 kJ・mol-1
2SO3(g) ΔH=?196.6 kJ・mol-1
2NO(g)+O2(g) 2NO2(g) ΔH =?113.0 kJ・mol-1
2NO2(g) ΔH =?113.0 kJ・mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH = kJ・mol-1。
SO3(g)+NO(g)的ΔH = kJ・mol-1。
一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO3的同时生成1 molNO2
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。该反应ΔH 0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。该反应ΔH 0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。

本题答案:(1)3NO2+H2O=NO+2HNO3;6.72;(2)-
本题解析:
试题分析:(1)二氧化氮与水反应生成一氧化氮和硝酸,6NO2中N元素化合价降低,由+4价降低到0价,则6molNO2参加反应,转移24mol电子,所以当转移1.2mol电子时,消耗NO20.3mol,体积为6.72L,故答案为:6.72;(2)已知:①2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1②2NO(g)+O2(g)?2NO2(g)△H=-113.0kJ?mol-1,利用盖斯定律,① ②
② 得NO2(g)+SO2(g)?SO3(g)+NO(g)△H=
得NO2(g)+SO2(g)?SO3(g)+NO(g)△H= (-196.6kJ?mol-1)-
(-196.6kJ?mol-1)- (-113.0kJ?mol-1)=-41.8kJ?mol-1,a.无论是否达到平衡,体系压强都保持不变,不能用于判断是否达到平衡状态,故a错误;b.混合气体颜色保持不变,说明浓度不变,达到平衡状态,故b正确;c.SO3和NO的计量数之比为1:1,无论是否达到平衡,二者的体积比保持不变,不能判断是否达到平衡状态,故c错误;d.物质的量之比等于化学计量数之比,则每消耗1mol SO3的同时生成1molNO2,不能判断是否达到平衡状态,故d错误.答案为:-41.8;b;(3)温度升高,CO的转化率降低,说明是放热反应,ΔH<0;在1.3×104kPa下,CO的转化率已经很高,如果增加压强CO的转化率提高不大,而生产成本增加较大,得不偿失。故答案为:< 在1.3×104kPa下,CO的转化率已经很高,如果增加压强CO的转化率提高不大,而生产成本增加较大,得不偿失。
(-113.0kJ?mol-1)=-41.8kJ?mol-1,a.无论是否达到平衡,体系压强都保持不变,不能用于判断是否达到平衡状态,故a错误;b.混合气体颜色保持不变,说明浓度不变,达到平衡状态,故b正确;c.SO3和NO的计量数之比为1:1,无论是否达到平衡,二者的体积比保持不变,不能判断是否达到平衡状态,故c错误;d.物质的量之比等于化学计量数之比,则每消耗1mol SO3的同时生成1molNO2,不能判断是否达到平衡状态,故d错误.答案为:-41.8;b;(3)温度升高,CO的转化率降低,说明是放热反应,ΔH<0;在1.3×104kPa下,CO的转化率已经很高,如果增加压强CO的转化率提高不大,而生产成本增加较大,得不偿失。故答案为:< 在1.3×104kPa下,CO的转化率已经很高,如果增加压强CO的转化率提高不大,而生产成本增加较大,得不偿失。
本题所属考点:【化学平衡】
本题难易程度:【困难】
Many hands make light work. 众擎易举. /人多好办事./ 众人拾柴火焰高.