微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (15分)甲醇是主要的化学工业基础原料和清洁液体燃料。工业上可以用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
化学反应及平衡常数
| 温度/℃
|
500
| 800
|
①2H2(g)+CO(g)  CH3OH(g) △H1 CH3OH(g) △H1
| K1
| 2.5
| 0.15
|
②H2(g)+CO2(g)  CO(g) +H2O(g) △H2 CO(g) +H2O(g) △H2
| K2
| 1.0
| 2.50
|
③3H2(g)+CO2(g)  CH3OH(g)+H2O(g) 91EXAM.org;△H3 CH3OH(g)+H2O(g) 91EXAM.org;△H3
| K3
|
|
|

(1)反应②的反应热△H2 0(填“>”、“<”或“=”);
(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系如图1所示。则平衡状态由A变到B时,平衡常数K(A)______K(B)(填“>”、“<”或“=”);
(3)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=___________(用K1、K2表示)。500℃时测得反应③在某时刻H2(g)、CO2(g) 、CH3OH(g)、H2O(g)的浓度(mol/L)分别为0.8、0.1、0.3、0.15,则此时v(正)______v(逆) (填“>”、“<”或“=”);
(4)在3L容积可变的密闭容器中发生反应②,已知c(CO)与反应时间t变化曲线Ⅰ如图2所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。当曲线Ⅰ变为曲线Ⅱ时,改变的条件是___________;当曲线Ⅰ变为曲线Ⅲ时,改变的条件是______________________________________;
(5)一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下,将amol/L的乙酸与bmol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)=c(CH3COO-),用含a和b的代数式表示该混合溶液中乙酸的电离常数为_________________________。
填空题 (15分)甲醇是主要的化学工业基础原料和清洁液体燃料。工业上可以用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
化学 反应及平衡常数
| 温度/℃
|
500
| 800
|
①2H2(g)+CO(g)  CH3OH(g) △H1 CH3OH(g) △H1
| K1
| 2.5
| 0.15
|
②H2(g)+CO2(g)  CO(g) +H2O(g) △H2 CO(g) +H2O(g) △H2
| K2
| 1.0
| 2.50
|
③3H2(g)+CO2(g)  CH3OH(g)+H2O(g) △H3 CH3OH(g)+H2O(g) △H3
| K3
|
|
|

(1)反应②的反应热△H2 0(填“>”、“<”或“=”);
(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系如图1所示。则平衡状态由A变到B时,平衡常数K(A)______K(B)(填“>”、“<”或“=”);
(3)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=___________(用K1、K2表示)。500℃时测得反应③在某时刻H2(g)、CO2(g) 、CH3OH(g)、H2O(g)的浓度(mol/L)分别为0.8、0.1、0.3、0.15,则此时v(正)______v(逆) (填“>”、“<”或“=”);
(4)在3L容积可变的密闭容器中发生反应②,已知c(CO)与反应时间t变化曲线Ⅰ如图2所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。当曲线Ⅰ变为曲线Ⅱ时,改变的条件是___________;当曲线Ⅰ变为曲线Ⅲ时,改变的条件是______________________________________;
(5)一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下,将amol/L的乙酸与bmol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)=c(CH3COO-),用含a和b的代数式表示该混合溶液中乙酸的电离常数为_________________________。
本题答案:(共15分)⑴ > (2分)⑵ =(2分)(3)K
本题解析:
试题分析:⑴由于反应②,升高温度,化学平衡常数增大,说明升高温度,平衡向正反应方向移动。根据平衡移动原理可知:正反应方向是吸热反应,所以△H2>0;(2)由于化学平衡常数只与温度有关,而与外界的压强、浓度等无关,如图显示的是反应①中H2的平衡转化率(a)与体系总压强(P)的关系由于温度不变,所以平衡状态由A变到B时,平衡常数K(A)= K(B);(3)根据反应的方程式可得化学平衡常数的表达式:K1=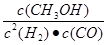 ;K2=
;K2=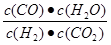 ;K3=
;K3=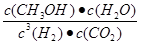 可推导出K1、K2与K3之间的关系,则K3= K1・K2;500℃时测得反应③的化学平衡常数K3=2.5×1.0=2.5,在某时刻H2(g)、CO2(g) 、CH3OH(g)、H2O(g)的浓度(mol/L)分别为0.8、0.1、0.3、0.15,Qc=
可推导出K1、K2与K3之间的关系,则K3= K1・K2;500℃时测得反应③的化学平衡常数K3=2.5×1.0=2.5,在某时刻H2(g)、CO2(g) 、CH3OH(g)、H2O(g)的浓度(mol/L)分别为0.8、0.1、0.3、0.15,Qc=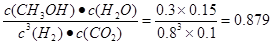 <2.5,说明反应还没有达到平衡状态,反应正向进行,此时v(正) >v(逆) ;(4)在3L容积可变的密闭容器中发生反应②,已知c(CO)与反应时间t变化曲线Ⅰ如图2所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。当曲线Ⅰ变为曲线Ⅱ时,由于反应速率加快,但是CO的平衡含量没有变化,及平衡未发生移动则改变的条件是加入催化剂;当曲线Ⅰ变为曲线Ⅲ时,CO浓度由原来的2mol/L 突然增大到3mol/L,CO的平衡浓度有原来的3mol/L变为4.5mol/L,都是原来曲线Ⅰ的1.5倍,则改变的条件是将容器的体积迅速压缩至2L;(5)一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下,将amol/L的乙酸与bmol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)=c(CH3COO-),则电离的醋酸的浓度是2bmol/L,醋酸的总浓度是amol/L,所以用含a和b的代数式表示该混合溶液中乙酸的电离常数为K=
<2.5,说明反应还没有达到平衡状态,反应正向进行,此时v(正) >v(逆) ;(4)在3L容积可变的密闭容器中发生反应②,已知c(CO)与反应时间t变化曲线Ⅰ如图2所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。当曲线Ⅰ变为曲线Ⅱ时,由于反应速率加快,但是CO的平衡含量没有变化,及平衡未发生移动则改变的条件是加入催化剂;当曲线Ⅰ变为曲线Ⅲ时,CO浓度由原来的2mol/L 突然增大到3mol/L,CO的平衡浓度有原来的3mol/L变为4.5mol/L,都是原来曲线Ⅰ的1.5倍,则改变的条件是将容器的体积迅速压缩至2L;(5)一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下,将amol/L的乙酸与bmol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)=c(CH3COO-),则电离的醋酸的浓度是2bmol/L,醋酸的总浓度是amol/L,所以用含a和b的代数式表示该混合溶液中乙酸的电离常数为K=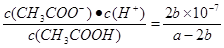 .
.
考点:考查化学平衡常数的计算、应用、化学反应进行的方向的判断、影响化学平衡的因素、物质的电离平衡常数的表达式的计算的知识。
本题所属考点:【化学平衡】
本题难易程度:【一般】
The wife is the key of the house. 妻子是一家的关键.