微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (15分)某硫酸厂用以下几种方法处理SO2尾气。
(1)活性炭还原法
反应原理:恒温恒容.2C (s)+2SO2(g) S2(g)+2CO2(g) 。
S2(g)+2CO2(g) 。
反应进行到不同时间测得各物质的浓度如图
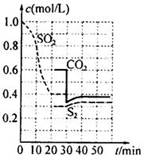
①第一次出现平衡的时间是第 min;
②0~20min反应速率表示为V(SO2)= ;
③30 min时,改变某一条件平衡发生移动,则改变的条件最有可能是 ;40min时,平衡常数值为____。
(2)亚硫酸钠吸牧法
①Na2SO3溶液吸收SO2的离子方程式为 ;
②常温下,当吸收至pH=6时,吸收液中相关离子浓度关系一定正确的是____(填序号)
a.c(Na+)+c(H+) >c(SO32-)+c(HSO3-)+ c(OH-)
b.c(Na+) = c(SO32-)+ c(HSO3-)+ C(H2SO3)
c.c(Na+)> c(SO32-)> c(OH一)>c(H+)
d.水电离出c(OH一)=l×l0-8 mol/L,
(3)电化学处理法
如图所示,Pt(1)电极的反应式为 ;碱性条件下,用P(2)电极排出的S2O42-溶液吸收NO2,使其转化为N2,同时有SO32-生成。若阳极转移电子6mol,则理论上处理NO2气体 mol。
填空题 (15分)某硫酸厂用以下几种方法处理SO2尾气。
(1)活性炭还原法
反应原理:恒温恒容.2C (s)+2SO2(g) S2(g)+2CO2(g) 。
S2(g)+2CO2(g) 。
反应进行到不同时间测得各物质的浓度如图

①第一次出现平衡的时间是第 min;
②0~20min反应速率表示为V(SO2)= ;
③30 min时,改变某一条件平衡发生移动,则改变的条件最有可能是 ;40min时,平衡常数值为____。
(2)亚硫酸钠吸牧法
①Na2SO3溶液吸收SO2的离子方程式为 ;
②常温下,当吸收至pH=6时,吸收液中相关离子浓度关系一定正确的是____(填序号)
a.c(Na+)+c(H+) >c(SO32-)+c(HSO3-)+ c(OH-)
b.c(Na+) = c(SO32-)+ c(HSO3-)+ C(H2SO3)
c.c(Na+)> c(SO32-)> c(OH一)>c(H+)
d.水电离出c(OH一)=l×l0-8 mol/L,
(3)电化学处理法
91eXaM.org如图所示,Pt(1)电极的反应式为 ;碱性条件下,用P(2)电极排出的S2O42-溶液吸收NO2,使其转化为N2,同时有SO32-生成。若阳极转移电子6mol,则理论上处理NO2气体 mol。
本题答案:(1)①20 (1分) ②0.03mol/(L・m
本题解析:
试题分析:(1)①根据图像可知,物质的浓度都不变的状态为平衡状态,所以第一次平衡的时间是20min时;
②0~20min反应速率表示为V(SO2)=(1.0-0.4)mol/L/20min="0.03" mol/(L・min);
③30 min时,图像中二氧化碳的浓度瞬间减小,所以可能改变的条件是减小二氧化碳的浓度;40min时,平衡常数值与20min时的平衡常数值相同,利用20min时各物质的浓度计算K=0.62×0.3/0.42=0.675;
(2)①Na2SO3溶液吸收SO2生成亚硫酸氢钠,离子方程式是SO32-+SO2+H2O=2HSO3-;
②a、根据电荷守恒,则c(Na+)+c(H+) =2c(SO32-)+c(HSO3-)+ c(OH-),所以c(Na+)+c(H+) >c(SO32-)+c(HSO3-)+ c(OH-),正确;b、pH=6时溶液呈酸性,则此时的溶液不一定恰好为亚硫酸氢钠溶液,所以Na元素与S元素不一定符合物料守恒,错误;c、因为溶液呈酸性,所以c(OH一)<c(H+),错误;d、pH=6,则溶液中的氢氧根离子浓度是10-8mol/L,氢氧根离子来自水的电离,所以水电离产生的氢氧根离子浓度是10-8mol/L,正确,答案选ad;
(3)根据装置图可知Pt(1)发生的是二氧化硫被氧化为硫酸的反应,所以该电极是负极,则Pt(1)电极的反应式为SO2-2e-+ 2H2O=SO42-+4H+;二氧化氮转化为氮气,N元素的化合价降低到0价,得到4个电子,根据得失电子守恒,则理论上处理NO2气体的物质的量是6mol/4=1.5mol。
考点:考查对图像的分析,反应速率的计算,平衡常数的计算,电化学反应原理的应用
本题所属考点:【化学平衡】
本题难易程度:【困难】
To insure peace of mind ignore the rules and regulations. 要想心安理得,就不要去管什么条条框框.