|
在373K 时,把0.5 mol N2O4气体通入体积为5L的密闭容器中发生反?【化学平衡】
选择题 在373K 时,把0.5 mol N2O4气体通入体积为5L的密闭容器中发生反应:N2O4(g) |

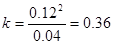 ,故A错误;N2O4的转化率为
,故A错误;N2O4的转化率为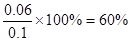 ,故B正确;前2s,NO2的平均反应速率为
,故B正确;前2s,NO2的平均反应速率为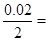 0.01mol・L-1・s-1,N2O4的平均反应速率为0.005mol・L-1・s-1,故C正确;2 s时,NO2的物质的量0.1mol,反应的N2O4的物质的量0.05mol,剩余N2O4的物质的量0.45mol・L-1,在2s时,体系内压强为反应前的1.1倍,故D正确。
0.01mol・L-1・s-1,N2O4的平均反应速率为0.005mol・L-1・s-1,故C正确;2 s时,NO2的物质的量0.1mol,反应的N2O4的物质的量0.05mol,剩余N2O4的物质的量0.45mol・L-1,在2s时,体系内压强为反应前的1.1倍,故D正确。本题所属考点:【化学平衡】
本题难易程度:【一般】
|
||
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | ||
| 下一篇:(11分)(1)据报道以硼氢化合物.. | ||