微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (共16分)
Ⅰ.(10分)已知2A(g)+B(g)  2C(g);△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为w mol/L,放出热量b kJ。
2C(g);△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为w mol/L,放出热量b kJ。
(1)比较a b( 填 > 、 = 、 < )
(2)若在原来的容器中,只加入2mol C,500℃时充分反应达平衡后,吸收热量ckJ,C物质的浓度 (填>、=、<)w mol/L,a、b、c之间满足的关系式为 (用含a、b、c的代数式表示)。
(3)能说明该反应已经达到平衡状态的是 。
a、V(C)=2V(B); b、容器内压强保持不变
c、V逆(A)=2V正(B) d、容器内的密度保持不变
(4)若将上述容器改为恒压容器(反应前体积相同),起始时加入2molA和lmolB,500℃时充分反应达平衡后,放出热量d kJ,则d b ( 填 > 、 = 、 < ),
Ⅱ.(6分)用吸收H2后的稀土储氢合金作为电池负极材料(用MH表示),
NiO(OH)作为电池正极材料,KOH溶液作为电解质溶液,可制得高容量,长寿命的镍氢电池。电池充放电时的总反应为:
NiO(OH)+MH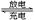 Ni(OH)2+M
Ni(OH)2+M
(1)电池放电时,负极的电极反应式为_______
(2)充电完成时,Ni(OH)2全部转化为NiO(OH)。若继续充电将在一个电极产生O2,O2扩散到另一个电极发生电极反应被消耗,从而避免产生的气体引起电池爆炸,此时,阴极的电极反应式为________。
填空题 (共16分)
Ⅰ.(10分)已知2A(g)+B(g)  2C(g);△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为w mol/L,放出热量b kJ。
2C(g);△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为w mol/L,放出热量b kJ。
(1)比较a b( 填 > 、 = 、 < )
(2)若在原来的容器中,只加入2mol C,500℃时充分反应达平衡后,吸收热量ckJ,C物质的浓度 (填>、=、<)w mol/L,a、b、c之间满足的关系式为 (用含a、b、c的代数式表示)。
(3)能说明该反应已经达到平衡状态的是 。
a、V(C)=2V(B); b、容器内压强保持不变
c、V逆(A)=2V正(B) d、容器内的密度保持不变
(4)若将上述容器改为恒压容器(反应前体积相同),起始时加入2molA和lmolB,500℃时充分反应达平衡后,放出热量d kJ,则d b ( 填 > 、 = 、 < ),
Ⅱ.(6分)用吸收H2后的稀土储氢合金作为电池负极材料(用MH表示),
NiO(OH)作为电池正极材料,KOH溶液作为电解质溶液,可制得高容量,长寿命的镍氢电池。电池充放电时的总反应为:
NiO(OH)+MH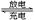 Ni(OH)2+M
Ni(OH)2+M
(1)电池放电时,负极的电极反应式为_______
(2)充电完成时,Ni(OH)2全部转化为NiO(OH)。若继续充电将在一个电极产生O2,O2扩散到另一个电极发生电极反应被消耗,从而避免产生的气体引起电池爆炸,此时,阴极的电极反应式为________。
本题答案:Ⅰ.(1)a > b
本题解析:
试题解析:Ⅰ.(1)已知2A(g)+B(g)?2C(g),△H="-a" kJ?mol-1(a>0),该反应为可逆反应,可逆反应中反应物不能全部转化为生成物,则在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为wmol/L,则w<2,所以放出热量为小于akJ,即a>b;(2)若在原来的容器中,只加入2molC,全部转化为AB分别为2molA和1molB,则与原平衡时等效平衡,平衡时浓度相同,所以平衡时C的浓度等于wmol/L;正向反应和逆向反应的转化率之和为100%,则正向反应放热与逆向反应放热之和为a kJ,所以a=b+c;(3)a.v(C)="2v" (B),从反应开始平衡一直有这样的等量关系,所以不能作平衡状态的标志,故a不选;b.容器内压强保持不变,说明总物质的量不变,正逆反应速率相等,故b选;c.v逆(A)=2v逆(B)=2v正(B2),说明达平衡状态,故c选;d.容器内的密度保持不变,从反应开始平衡一直有这样的等量关系,所以不能作平衡状态的标志,故d不选;故选:bc; (4)恒压条件下,由于始终保持较大压强,转化的越多,放出热量较多,则d > b 。Ⅱ. (1)负极反应物MH失去电子,生成的H+在碱性条件下生成H2O,电解反应式为 :MH-e-+OH-=H2O+M;(2)阴极的电极反应有两个,第一阶段是充电时的反应式,阴极上电极反应式为M+H2O+e-
本题所属考点:【化学平衡】
本题难易程度:【一般】
What may be done at any time is done at no time. 随时可做的事,往往没时间做.