|
|
|
(12分)在一容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,【化学平衡】
2016-12-26 18:12:10
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (12分)在一容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g) 2NH3(g)△H<0,反应中NH3的浓度变化如下图: 2NH3(g)△H<0,反应中NH3的浓度变化如下图:
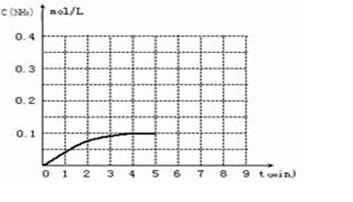
(1)根据上图,4min~5min之间,反应处于_________状态;(填“平衡”或“非平衡”)。
计算0~4min内,平均反应速率υ(NH3)= 。
(2)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,来源:91考试网 91EXAm.org反应达到新平衡后,则NH3的物质的量浓度不可能为 。
A.0.2mol・L-1
B.0.12mol・L-1
C.0.10mol・L-1
D.0.08mol・L-1
| (3)反应达到平衡后,第5分钟末,保持其它条件不变,把容器的体积缩小为原来的一半,则平衡________________移动(填“向逆反应方向”、“向正反应方向”或“不”),化学平衡常数________(填“增大”、“减小”或“不变”)。
(4)在第5分钟末,将容器体积缩小为原来的一半后,若在第8分钟末达到新的平衡时(此时NH3的浓度约为0.25mol・L-1)。请在上图中画出第5分钟末到平衡时NH3浓度的变化曲线。
填空题 (12分)在一容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)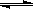 2NH3(g)△H<0,反应中NH3的浓度变化如下图: 2NH3(g)△H<0,反应中NH3的浓度变化如下图:

(1)根据上图,4min~5min之间,反应处于_________状态;(填“平衡”或“非平衡”)。
计算0~4min内,平均反应速率υ(NH3)= www.91exAm.org; 。
(2)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,反应达到新平衡后,则NH3的物质的量浓度不可能为 。
A.0.2mol・L-1
B.0.12mol・L-1
C.0.10mol・L-1
D.0.08mol・L-1
|
(3)反应达到平衡后,第5分钟末,保持其它条件不变,把容器的体积缩小为原来的一半,则平衡________________移动(填“向逆反应方向”、“向正反应方向”或“不”),化学平衡常数________(填“增大”、“减小”或“不变”)。
(4)在第5分钟末,将容器体积缩小为原来的一半后,若在第8分钟末达到新的平衡时(此时NH3的浓度约为0.25mol・L-1)。请在上图中画出第5分钟末到平衡时NH3浓度的变化曲线。
本题答案:(1)平衡(2分)0.025mol・L-1・min-1(2分
本题解析:
试题分析:(1)4-5分钟时氨气的浓度不变,说明反应到达平衡。 氨气的反应速率=01/4=0.025mol・L-1・min-1(2)若氮气和氢气完全反应生成氨气的浓度为0.2mol/L,但由于是可逆反应,物质不可能完全转化,所以氨气的浓度不可能为0.2mol/L,原平衡时氨气的浓度为0.1mol/L,改变温度,平衡肯定移动,所以氨气的浓度不可能是0.1mol/L。所以选A、C。(3)其它条件不变,容器的体积缩小,是加压,平衡向正反应方向移动,由于温度不变,所以平衡常数不变。
(4)将容器的体积缩小到一半,则浓度都变成原来的2倍,平衡正向移动,氮气和氢气的浓度逐渐减小,氨气的浓度逐渐增大,所以得到图像
考点:化学平衡常数的应用,化学平衡移动。
本题所属考点:【化学平衡】
本题难易程度:【一般】
If you would know the value of money, go and try to borrow some. 要想知道钱的价值,就想办法去借钱试试.