微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (17分)利用天然气可制得以H2、CO等为主要组成的工业原料合成气,反应为:CH4(g)+H2O(g) CO(g)+3H2(g)。
CO(g)+3H2(g)。
(1)甲烷与水蒸气反应,被氧化的元素是 ,当生成标准状况下35.84L合成气时转移电子的物质的量是 。
(2)将2 mol CH4和5 mol H2O(g)通入容积为100L的反应室,CH4的平衡转化率与温度、压强的关系如图。
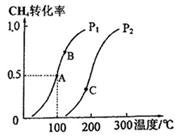
①达到A点所需的时间为5min,则v(H2)= ,100℃时平衡常数K= 。
②图中的Pl P2(填“<”、“>”或“=”),A、B、C三点的平衡常数KA、KB、KC的大小关系是 。
(3)合成气用于合成氨气时需除去CO,发生反应CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)  H<0,
H<0,
下列措施中能使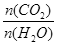 增大的 (选填编号)。
增大的 (选填编号)。
A.降低温度 来源:91 考试网 B.恒温恒容下充入He(g)
C.将H2从体系中分离 D.再通入一定量的水蒸气
可用碳酸钾溶液吸收生成的CO2,常温下pH=10的碳酸钾溶液中水电离的OH-的物质的量浓度为 ,常温下,0.1 mol・L-1KHCO3溶液pH>8,则溶液中c(H2CO3) c(CO32-)(填“>”、“=”或“<”)。
填空题 (17分)利用天然气可制得以H2、CO等为主要组成的工业原料合成气,反应为:CH4(g)+H2O(g) CO(g)+3H2(g)。
CO(g)+3H2(g)。
(1)甲烷与水蒸气反应,被氧化的元素是 ,当生成标准状况下35.84L合成气时转移电子的物质的量是 。
(2)将2 mol CH4和5 mol H2O(g)通入容积为100L的反应室,CH4的平衡转化率与温度、压强的关系如图。

①达到A点所需的时间为5min,则v(H2)= ,100℃时平衡常数K= 。
②图中的Pl P2(填“<”、“>”或“=”),A、B、C三点的平衡常数KA、KB、KC的大小关系是 。
(3)合成气用于合成氨气时需除去CO,发生反应CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)  H<0,
H<0,
下列措施中能使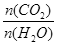 增大的 (选填编号)。
增大的 (选填编号)。
A.降低温度 B.恒温恒容下充入He(g)
C.将H2从体系中分离 D.再通入一定量的水蒸气
可用碳酸钾溶液吸收生成的CO2,常温下pH=10的碳酸钾溶液中水电离的OH-的物质的量浓度为 ,常温下,0.1 mol・L-1KHCO3溶液pH>8,则溶液中c(H2CO3) c(CO32-)(填“>”、“=”或“<”)。
本题答案:(17分)(1)C(碳)(1分) 2
本题解析:
试题分析:(1)甲烷与水蒸气反应,甲烷中的碳元素由-4价变为反应后CO中的+2价,化合价升高,失去电子被氧化。因此被氧化的元素是C;根据方程式可知,每产生4mol的气体,转移电子的物质的量是6mol的电子,现在得到的气体的物质的量是:n=35.84L÷22.4L/mol=1.6mol,所以转移电子的物质的量是n(e-)="(1.6mol÷4)" ×6=2.4mol;(2)①由于CH4的转化率是0.5,所以发生反应消耗的甲烷的物质的量是2 mol×0.5=1mol,根据方程式可知,每有1mol的甲烷反应,会产生3mol 的氢气,所以v(H2)=3mol÷100L÷5min=0.006mol・L-1・min-1;在100℃时,反应达到平衡时,各种物质的浓度分别是:c(CH4)=0.01mol/L;c(H2O)=0.04mol/L;c(CO)=0.01mol/L;c(H2)=0.03mol/L,所以该反应的平衡常数是: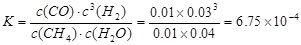 ;②根据图像可知:在温度不变时,在压强为p1时CO的转化率大于p2时CO的转化率,由于该反应的正反应为气体体积增大的反应,所以在温度不变时,减小压强,平衡向气体体积增大的正反应方向移动,所以压强:Pl <P2;(3)CO(g)+H2O(g)
;②根据图像可知:在温度不变时,在压强为p1时CO的转化率大于p2时CO的转化率,由于该反应的正反应为气体体积增大的反应,所以在温度不变时,减小压强,平衡向气体体积增大的正反应方向移动,所以压强:Pl <P2;(3)CO(g)+H2O(g) CO2(g)+H2(g)的正反应为放热反应,A.降低温度,平衡向放热反应方向移动,n(CO2)增大,n(H2O)减小,所以n(CO2)/ n(H2O)增大,正确;B.恒温恒容下充入He(g),由于物质的浓度都不变,所以平衡不发生移动,n(CO2)/ n(H2O)不变,错误;C.将H2从体系中分离,减小生成物的浓度,平衡正向移动,n(CO2)增大,n(H2O)减小,所以n(CO2)/ n(H2O)增大,正确;D.再通入一定量的水蒸气,即增大反应物的浓度,平衡正向移动,n(CO2)增大,n(H2O)增大,而且平衡移动趋势是微弱的,所以n(CO2)/ n(H2O)反而减小,错误。故正确选项是AC;常温下pH=10的碳酸钾溶液中,c(H+)=10-10mol/L,则c(OH-)=10-4mol/L,水 溶液中的OH-就是水电离产生的,所以水电离的OH-的物质的量浓度为10-4mol/L;在1KHCO3溶液中存在HCO3-的水解作用和它的电离作用,电离产生H+使溶液显酸性;水解消耗H+,使溶液显碱性,由于0.1 mol・L-1KHCO3溶液pH>8,则说明HCO3-的水解作用大于电离作用,所以溶液中c(H2CO3)>c(CO32-)。
CO2(g)+H2(g)的正反应为放热反应,A.降低温度,平衡向放热反应方向移动,n(CO2)增大,n(H2O)减小,所以n(CO2)/ n(H2O)增大,正确;B.恒温恒容下充入He(g),由于物质的浓度都不变,所以平衡不发生移动,n(CO2)/ n(H2O)不变,错误;C.将H2从体系中分离,减小生成物的浓度,平衡正向移动,n(CO2)增大,n(H2O)减小,所以n(CO2)/ n(H2O)增大,正确;D.再通入一定量的水蒸气,即增大反应物的浓度,平衡正向移动,n(CO2)增大,n(H2O)增大,而且平衡移动趋势是微弱的,所以n(CO2)/ n(H2O)反而减小,错误。故正确选项是AC;常温下pH=10的碳酸钾溶液中,c(H+)=10-10mol/L,则c(OH-)=10-4mol/L,水 溶液中的OH-就是水电离产生的,所以水电离的OH-的物质的量浓度为10-4mol/L;在1KHCO3溶液中存在HCO3-的水解作用和它的电离作用,电离产生H+使溶液显酸性;水解消耗H+,使溶液显碱性,由于0.1 mol・L-1KHCO3溶液pH>8,则说明HCO3-的水解作用大于电离作用,所以溶液中c(H2CO3)>c(CO32-)。
考点:考查氧化还原反应的有关概念、化学反应速率、化学平衡的有关计算、盐的水解和电离的知识。
本题所属考点:【化学平衡】
本题难易程度:【困难】
A brave man risks his life, but not his conscience. 勇敢的人可用生命冒险,但不以良心冒险。