|
(1)如图所示,烧杯甲中盛放100 mL 6 mol・L-1的HCl溶液,烧杯【化学平衡】
F.c(NO2)=2 c(N2O4) 填空题 (1)如图所示,烧杯甲中盛放100 mL 6 mol・L-1的HCl溶液,烧杯乙中盛放100 mL冷水,现向烧杯甲的溶液中放入NaOH固体,同时向烧 杯乙中放入NH4NO3固体,搅拌使之溶解。A瓶中气体颜色变深,B瓶气体颜色变浅,理由是: 。 |
 N2O4(g) △H<0,NaOH中和HCl时要放热,平衡向左移动,NO2浓度增大,颜色加深。NH4NO3溶解吸热,温度降低,平衡向右移动,NO2浓度减小,气体颜色变浅”。(2)根据反应速率之比等于方程式中系数之比:X:Y=
N2O4(g) △H<0,NaOH中和HCl时要放热,平衡向左移动,NO2浓度增大,颜色加深。NH4NO3溶解吸热,温度降低,平衡向右移动,NO2浓度减小,气体颜色变浅”。(2)根据反应速率之比等于方程式中系数之比:X:Y= :
: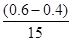 =2:1,X表示NO2浓度随时间的变化,填:“X”;②v(N2O4)=
=2:1,X表示NO2浓度随时间的变化,填:“X”;②v(N2O4)=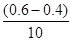 mol/(L・min)=0.02mol/(L・min);③25min时NO2的浓度突然增大,而N2O4的浓度不变,说明改变的因素不是温度、压强、催化剂,只能是增大了NO2的浓度,填写“在容器中添加了NO2”;④N2O4
mol/(L・min)=0.02mol/(L・min);③25min时NO2的浓度突然增大,而N2O4的浓度不变,说明改变的因素不是温度、压强、催化剂,只能是增大了NO2的浓度,填写“在容器中添加了NO2”;④N2O4 2NO2,10min的平衡常数k=
2NO2,10min的平衡常数k=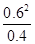 =0.9,平衡常数只受温度的影响,温度不变,平衡常数不变,即35min时平衡常数仍是0.9;⑤A、等容状态下,反应前后的气体系数之和不相等,压强随反应的进行减小,当压强不再改变说明达到了平衡,不符合题意;B、NO2红棕色气体,N2O4无色,当颜色不再改变,说明反应达到平衡状态,不符合题意;C、M=
=0.9,平衡常数只受温度的影响,温度不变,平衡常数不变,即35min时平衡常数仍是0.9;⑤A、等容状态下,反应前后的气体系数之和不相等,压强随反应的进行减小,当压强不再改变说明达到了平衡,不符合题意;B、NO2红棕色气体,N2O4无色,当颜色不再改变,说明反应达到平衡状态,不符合题意;C、M=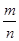 ,反应前后都是气体,遵循质量守恒,m不变,反应前后气体系数之和不等,M不再改变,说明反应达到平衡状态,不符合题意;D、ρ=
,反应前后都是气体,遵循质量守恒,m不变,反应前后气体系数之和不等,M不再改变,说明反应达到平衡状态,不符合题意;D、ρ= ,m不变,容器是等容的,v不变,ρ不变,不能作为达到平衡的标志;E、速率表示反应达到平衡的标志,要求方向是一正一逆,问题没有说明,所以此速率的关系不能作为达到平衡的标志;F、同E的分析,因此不能作为达到平衡标志的是:DEF。
,m不变,容器是等容的,v不变,ρ不变,不能作为达到平衡的标志;E、速率表示反应达到平衡的标志,要求方向是一正一逆,问题没有说明,所以此速率的关系不能作为达到平衡的标志;F、同E的分析,因此不能作为达到平衡标志的是:DEF。
CH3
 3
3 CH3
CH3 CH3
CH3 CH3
CH3 C
C CH
CH CH
CH CH2
CH2本题所属考点:【化学平衡】
本题难易程度:【困难】
|
||
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | ||
| 下一篇:恒温条件下,往容积为2L的密闭容.. | ||