微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 在一体积为10L的密闭客器中,通入一定量的CO和H2O,在85℃发生如下反应:
CO (g)+H2O(g) 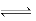 CO2(g)+H2(g) △H<O。
CO2(g)+H2(g) △H<O。
CO和H2O浓度变化如图所示:

请回答下列问题:
(1)能判断该反应达到化学平衡状态的依据是___________________(填选项序号)。
a.容器中压强不变
b.混合气体中c(CO)不变
c.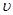 正(H2)=
正(H2)= 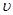 逆(H2O)
逆(H2O)
d.c(CO2)=c(CO)
e.容器中气体密度不变
f.1 mol H-H键断裂的同时断裂2 mol H-O键
(2)①0~4min内的平均反应速率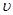 (CO)=___________mol・L―1・min―1;
(CO)=___________mol・L―1・min―1;
②85℃时,该反应化学平衡常数K=____________。
(3)85℃时,若起始时向该容器中充入1.0 molCO、3.0 molH2O,则此时CO的平衡转化率为______________。 91eXAm.org
填空题 在一体积为10L的密闭客器中,通入一定量的CO和H2O,在85℃发生如下反应:
CO (g)+H2O(g) 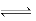 CO2(g)+H2(g) △H<O。
CO2(g)+H2(g) △H<O。
CO和H2O浓度变化如图所示:

请回答下列问题:
(1)能判断该反应达到化学平衡状态的依据是___________________(填选项序号)。
a.容器中压强不变
b.混合气体中c(CO)不变
c.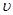 正(H2)=
正(H2)= 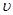 逆(H2O)
逆(H2O)
d.c(CO2)=c(CO)
e.容器中气体密度不变
f.1 mol H-H键断裂的同时断裂2 mol H-O键
(2)①0~4min内的平均反应速率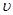 (CO)=___________mol・L―1・min―1;
(CO)=___________mol・L―1・min―1;
②85℃时,该反应化学平衡常数K=____________。
(3)85℃时,若起始时向该容器中充入1.0 molCO、3.0 molH2O,则此时CO的平衡转化率为______________。
本题答案:(1)b、c、f;(2)①0.03,②1;(3)75%
本题解析:
试题分析:(1)a、根据反应方程式,得知:反应前后气体系数之和相等,说明反应前后气体物质的量不变,根据压强比等于物质的量之比,也就是说任何时刻压强都相等,因此压强不能作为达到平衡的标志,错误;b、根据化学平衡状态的定义:一定条件下,可逆反应中,反应速率和生成速率相等且各组分的浓度不变的状态,混合气体c(CO)不变,可以证明反应达到了平衡,正确;c、不同物质的速率表示达到平衡的标志:反应方向是一正一逆,速率之比等于系数之比,v正(H2)是生成H2的速率向正反应方向进行,因H2O是反应物,v逆(H2O)向生成H2O的方向进行,向逆反应进行,H2、H2O的系数相等,v正(H2)=v逆(H2O)能说明反应达到化学平衡,正确;d、不知开始投入量是多少,转化率是多少,c(CO2)=c(CO)不能说明反应达到平衡,错误;e、ρ=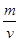 ,组分都是气体,根据质量守恒定律,反应前后质量不变(m不变),条件是等容条件(v不变),ρ不能作为达到平衡的标志,错误;f、1molH-H断裂,1molH2含1molH-H,说明反应是向消耗H2的反应进行,即逆反应方向进行,2molH-O断裂说明反应向 正反应方向进行,1molH2O含2molH-O,断裂2molH-O有1mol的H2O被消耗,符合“用速率作为平衡标志的条件”,正确;(2)①根据反应速率的定义:
,组分都是气体,根据质量守恒定律,反应前后质量不变(m不变),条件是等容条件(v不变),ρ不能作为达到平衡的标志,错误;f、1molH-H断裂,1molH2含1molH-H,说明反应是向消耗H2的反应进行,即逆反应方向进行,2molH-O断裂说明反应向 正反应方向进行,1molH2O含2molH-O,断裂2molH-O有1mol的H2O被消耗,符合“用速率作为平衡标志的条件”,正确;(2)①根据反应速率的定义: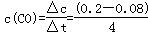 mol/(L・min)=0.03mol/(L・min);②CO(g)+H2O(g)
mol/(L・min)=0.03mol/(L・min);②CO(g)+H2O(g) CO2(g)+H2(g),根据浓度变化图,得知消耗的CO、H2O的浓度是0.12mol・L-1,则生成的CO2、H2的浓度是0.12mol・L-1,
CO2(g)+H2(g),根据浓度变化图,得知消耗的CO、H2O的浓度是0.12mol・L-1,则生成的CO2、H2的浓度是0.12mol・L-1,
K=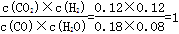 ;(3)温度不变,平衡常数不变,设反应了CO为xmol
;(3)温度不变,平衡常数不变,设反应了CO为xmol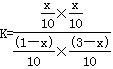 ="1" ,解得x=0.75,则CO的转化率=
="1" ,解得x=0.75,则CO的转化率= ×100%=75%。
×100%=75%。
考点:考查达到化学平衡的标志、化学反应速率的计算、平衡常数等相关知识。
本题所属考点:【化学平衡】
本题难易程度:【困难】
Calf love,half love; old love, cold love. 童年相爱,半是稚气; 老年相爱,爱得深沉.