微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (6分)某温度下,将4.0 mol的HI气体充入1 L已经抽空的固定容积的密闭容器中,发生如下反应:2HI(g)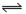 H2(g)+I2(g) ΔH>0,隔一段时间对该容器内的物质进行分 91ExAM.org析,得到如下数据:
H2(g)+I2(g) ΔH>0,隔一段时间对该容器内的物质进行分 91ExAM.org析,得到如下数据:
时间/s
n /mol
| 0
| 40
| 80
| 120
|
n(HI)
| 4.0
| 2.8
| b
| c
|
n(H2)
| 0
| a
| 1.0
| 1.0
|
(1)a = ,c = ;
(2)计算在该温度时此反应的平衡常数K = ;
(3)保持温度不变,120 s时再通入2.0 mol的H2。当再次达到平衡时,HI的平衡转化率是多少?(本小题要有适当的解题过程)
填空题 (6分)某温度下,将4.0 mol的HI气体充入1 L已经抽空的固定容积的密闭容器中,发生如下反应:2HI(g)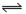 H2(g)+I2(g) ΔH>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
H2(g)+I2(g) ΔH>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
时间/s
n /mol
| 0
| 40
| 80
| 120
|
n(HI)
| 4.0
| 2.8
| b
| c
|
n(H2)
| 0
| a
| 1.0
| 1.0
|
(1)a = ,c = ;
(2)计算在该温度时此反应的平衡常数K = ;
(3)保持温度不变,120 s时再通入2.0 mol的H2。当再次达到平衡时,HI的平衡转化率是多少?(本小题要有适当的解题过程)
本题答案:(6分)(1)0.6(1分);2.0(1分);(2)K=0.
本题解析:
试题分析:(1)根据方程式2HI(g)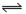 H2(g)+I2(g)可知,每发生反应消耗2mol的HI,现在产生1.0mol的H2、1mol的Cl2,现在反应消耗4.0mol-2.8mol=1.2mol,则会产生0.6mol的H2、0.6mol的Cl2;若反应产生1.0mol的H2、1.0mol的Cl2;会反应消耗2mol的2mol的HI,还有剩余的HI的物质的量是2.0mol,所以a=0.6mol;b=2.0mol;(2)由于反应在80s、120s时物质的量都不发生变化,所以反应处于平衡状态,则在该温度时此反应的平衡常数
H2(g)+I2(g)可知,每发生反应消耗2mol的HI,现在产生1.0mol的H2、1mol的Cl2,现在反应消耗4.0mol-2.8mol=1.2mol,则会产生0.6mol的H2、0.6mol的Cl2;若反应产生1.0mol的H2、1.0mol的Cl2;会反应消耗2mol的2mol的HI,还有剩余的HI的物质的量是2.0mol,所以a=0.6mol;b=2.0mol;(2)由于反应在80s、120s时物质的量都不发生变化,所以反应处于平衡状态,则在该温度时此反应的平衡常数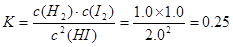 ;(3)保持温度不变,120 s时再通入2.0 mol的H2。平衡逆向移动,假如达到平衡时,c(I2)=xmol/L,则c(HI)=(4-2x)mol/L,c(H2)=(2.0+x)mol/L由于温度不变,所以化学平衡常数不变,因此
;(3)保持温度不变,120 s时再通入2.0 mol的H2。平衡逆向移动,假如达到平衡时,c(I2)=xmol/L,则c(HI)=(4-2x)mol/L,c(H2)=(2.0+x)mol/L由于温度不变,所以化学平衡常数不变,因此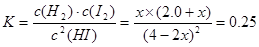 ,解得
,解得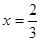 ,所以当再次达到平衡时,HI的平衡转化率是
,所以当再次达到平衡时,HI的平衡转化率是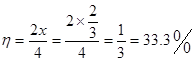 。
。
考点:考查本题考查了反应过程中物质的量、化学平衡常数的计算及物质平衡 转化率的计算的知识。
本题所属考点:【化学平衡】
本题难易程度:【困难】
It is better to give than to take. 施比受更有福.