微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (11分)工业上将煤气化过程中生成的CO和H2在一定条件下反应制得甲醇,反应的方程式为:CO(g)+2H2(g) CH3OH(g)。请根据图示回答下列问题:
CH3OH(g)。请根据图示回答下列问题:
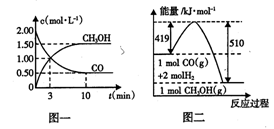
(1)从反应开始到平衡,用H2浓度变化表示的平均反应速率v(H2) =____ ;平衡时CO的转化率为____ 。
(2)该反应的平衡常数表达式为 ;若升高反应温度,该反应的平衡常数将 (填“增大”、“减小”或“不变”)。
(3)若在一定温度下,向一恒压容器中充人1 mol CO、2mol H2和1 mol CH3OH,反应达到平衡时,测得混合气体的密度是同温同压下起始混合气体密度的0.8倍,则到达平衡状态前该反应向____ (填“正”或“逆”)反应方向进行。
(4)根据图二,甲醇分解的热化学方程式为 。
(5)若以甲醇为原料制成燃料电池,在碱性介质中负极的电极反应式为____ 。
填空题 (11分)工业上将煤气化过程中生成的CO和H2在一定条件下反应制得甲醇,反应的方程式为:CO(g )+2H2(g) CH3OH(g)。请根据图示回答下列问题:
CH3OH(g)。请根据图示回答下列问题:
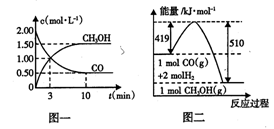
(1)从反应开始到平衡,用H2浓度变化表示的平均反应速率v(H2) =____ ;平衡时CO的转化率为____ 。
(2)该反应的平衡常数表达式为 ;若升高反应温度,该反应的平衡常数将 (填“增大”、“减小”或“不变”)。
(3)若在一定温度下,向一恒压容器中充人1 mol CO、2mol H2和1 mol CH3OH,反应达到平衡时,测得混合气体的密度是同温同压下起始混合气体密度的0.8倍,则到达平衡状态前该反应向____ (填“正”或“逆”)反应方向进行。
(4)根据图二,甲醇分解的热化学方程式为 。
(5)若以甲醇为原料制成燃料电池,在碱性介质中负极的电极反应式为____ 。
本题答案:(1)0.3 mol/(L?min) ,75% (2)c(C
本题解析:
试题分析:(1)从反应开始到平衡,用CO浓度变化表示的平均反应速v(CO)=(2.00-0.50)mol/L÷10min=0.15mol/(L?min);由于v(H2)=2V(CO),所以v(H2)=" 0.3" mol/(L?min);平衡时CO的转化率为(1.5mol/L÷2.00mol/L)×100%=75%,(2)该反应的平衡常数表达式为K=c(CH3OH)/c(CO)・c2(H2),由于反应物的能量高于生成物,所以该反应是放热反应。根据平衡移动原理,若升高反应温度,平衡向吸热的逆反应方向移动,该反应的平衡常数将减小;(3)由于反应前后气体的质量不变,若在一定温度下,向一恒压容器中充人1 mol CO、2mol H2和1 mol CH3OH,反应达到平衡时,测得混合气体的密度是同温同压下起始混合气体密度的0.8倍,密度减小,说明反应后气体的体积增大,反应逆向进行,为使越强与原来相等就应该扩大容器的容积,故到达平衡状态前该反应向逆反应方向进行。(4)根据图二可知1mol的甲醇分解产生1mol的CO和2mol的H2,反应需要吸热(510-419)KJ=91 KJ,所以甲醇分解的热化学方程式为CH3OH(g)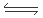 CO(g)+2H2(g) ΔH="+91" KJ/mol ;(5)若以甲醇为原料制成燃料电池,通入甲醇的电极为负极,在碱性介质中负极的电极反应式为CH3OH+8OH- -6e-=CO32-+6H2O。
CO(g)+2H2(g) ΔH="+91" KJ/mol ;(5)若以甲醇为原料制成燃料电池,通入甲醇的电极为负极,在碱性介质中负极的电极反应式为CH3OH+8OH- -6e-=CO32-+6H2O。
考点:考查化学反应速率的计算、物质的平衡转化率、反应进行的方向的判断、热化学方程式的书写及原电池反应的电极式的书写的知识。
本题所属考点:【化学反应速率】
本题难易程度:【困难】
Courage and resolution are the spirit and soul of virtue. 勇敢和坚定是美德的灵魂.