微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 已知0.4 mol液态肼(N2H4)与过量的液态双氧水反应,生成氮气和水蒸气,放出256.65 kJ的热量,该反应的热化学方程式为 ; 。
又已知:H2O(l)=H2O(g) ΔH =+44 kJ/mol,则16 g液态肼与液态双氧水反应生成液态水时放出的热量是 。
填空题 已知0.4 mol液态肼(N2H4)与过量的液态双氧水反应,生成氮气和水蒸气,放出256.65 kJ的热量,该反应的热化学方程式为 & 91EXAM.org#160; 。
又已知:H2O(l)=H2O(g) ΔH =+44 kJ/mol,则16 g液态肼与液态双氧水反应生成液态水时放出的热量是 。
本题答案:N2H4(l)+2H2O2(l)=N2(g)+4H2O(g)
本题解析:考查热化学方程式的书写。1mol液态肼放出的热量是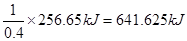 ,所以热化学方程式为N2H4(l)+2H2O2(l)=N2(g)+4H2O(g) ΔH=-641.625 kJ/mol;16g液态肼是0.5mol,生成气态水时放出的热量是0.5mol×641.625 kJ/mol=320.8125kJ,生成的2mol水变成液态又放出88kJ热量,所以最终放出的热量是320.8125kJ+88kJ=408.813 kJ.
,所以热化学方程式为N2H4(l)+2H2O2(l)=N2(g)+4H2O(g) ΔH=-641.625 kJ/mol;16g液态肼是0.5mol,生成气态水时放出的热量是0.5mol×641.625 kJ/mol=320.8125kJ,生成的2mol水变成液态又放出88kJ热量,所以最终放出的热量是320.8125kJ+88kJ=408.813 kJ.
本题所属考点:【热化学方程式】
本题难易程度:【一般】
Open different locks with different keys. 一把钥匙开一把锁。