|
|
|
运用盖斯定律可方便地计算出难以通过实验直接测定的反应热。已知【热化学方程式】
2016-12-26 23:36:24
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 运用盖斯定律可方便地计算出难以通过实验直接测定的反应热。已知:
①P4(白磷,s)+5O2(g)=P4O10(s) ΔH=-2983.2kJ・mol-1
②P(红磷,s)+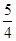 O2(g)= O2(g)=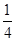 P4O10(s) ΔH=-738.5kJ・mol-1 P4O10(s) ΔH=-738.5kJ・mol-1
则白磷转化为红磷的热化学方程式为
A.P4(白磷,s)=4P(红磷,s) △H=-29.2kJ・mol-1
B.P4(白磷,s)=4P(红磷,s) △H=+29.2kJ・mol-1
C.P4(白磷,s)=4P(红磷,s) △H=-2244.7kJ・mo l-1
D.P4(白磷,s)=4P(红磷,s) △H=+2244.7kJ・mol-1
|
选择题 运用盖斯定律可方便地计算出难以通过实验直接测定的反应热。已知:
①P4(白磷,s)+5O2(g)=P4O10(s) ΔH=-2983.2kJ・mol-1
②P(红磷,s)+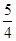 O2(g)= O2(g)=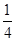 P4O10(s) ΔH=-738.5kJ・mol-1 P4O10(s) ΔH=-738.5kJ・mol-1
则白磷转化为红磷的热化学方程式为
A.P4(白磷,s)=4P(红磷,s) △H=-29.2kJ・mol-1
B.P4(白磷,s)=4P(红磷,s) △H www.91eXam.org=+29.2kJ・mol-1
C.P4(白磷,s)=4P(红磷,s) △H=-2244.7kJ・mol-1
D.P4(白磷,s)=4P(红磷,s) △H=+2244.7kJ・mol-1
|
本题答案:A
本题解析:
试题分析:将第二个式子扩大4倍,可得③4P(红磷,s)+5O2(g)=P4O10(s) ΔH=-2954kJ・mol-1.可见等质量的白磷比红磷含有的能量高,物质含有的能量越高,物质的稳定性就越强。①―③,整理可得P4(白磷,s)=4P(红磷,s) △H=-29.2kJ・mol-1,所以选项是A。
考点:考查热化学方程式的应用的知识。
本题所属考点:【热化学方程式】
本题难易程度:【一般】
Make yourself necessary to someone. 使自己成为别人需要的人.