|
|
|
已知:2H2(g) +O2(g) = 2H2O(g) ΔH =-483.6 kJ/mol <b【热化学方程式】
2016-12-26 23:44:27
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 ; 已知:2H2(g) +O2(g) = 2H2O(g) ΔH =-483.6 kJ/mol
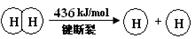
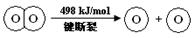
下列说法不正确的是
A.该反应原理可用于设计氢氧燃料电池
B.破坏1 mol H―O 键需要的能量是463.4 kJ
C.H2O(g)=H2(g) + 1/2O2(g) ΔH = +241.8 kJ/mol
D.H2(g) 中的H―H 键比 H2O(g) 中的H―O 键牢固
|
选择题 已知:2H2(g) +O2(g) = 2H2O(g) ΔH =-483.6 kJ/mol

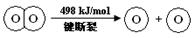
下列说法不正确的是
A.该反应原理可用于设计氢氧燃料电池
B.破坏1 mol H―O 键需要的能量是463.4 kJ
C.H2O(g)=H2(g) + 1/2O2(g) ΔH = +241.8 kJ/mol
D.H2(g) 中的H―H 键比 H2O(g) 中的H―O 键牢固
|
本题答案:D
本题解析:
试题分析:A、该反应为氧化还原反应,且是放热反应,故能设计成原电池,A正确;反应热=反应物的总键能-生成物的总键能=436x2+498-4x=-483.6,x=241.8,故B正确;2H2(g) +O2(g) = 2H2O(g),ΔH =-483.6 kJ/mol ,故逆反应吸收热量为+483.6kJ/mol,1mol水分解吸收热量为241.8 kJ/mol,C正确;键能越大越稳定,故H2(g) 中的H―H 键不如 H2O(g) 中的H―O 键牢固,D错误。答案选D
考点:反应热与原电池原理
本题所属考点:【热化学方程式】
本题难易程度:【一般】
Misfortunes tell us what fortune is. 不经灾难不知福.