微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
来源:91考试 网填空题 (14分)实验室测量KMnO4溶液浓度时常用(NH4)2Fe(SO4)2代替FeSO4作标液,(NH4)2Fe(SO4)2的制备工艺流程如下:
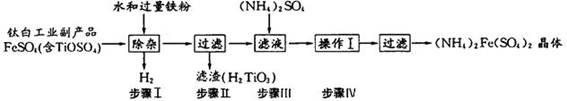
(1)已知流程中铁粉制备反应如下:
4 H2 O(g) +3Fe(s) Fe3O4(s)十4H2(g) △H ="a" kJ /mol
Fe3O4(s)十4H2(g) △H ="a" kJ /mol
Fe3O4(s) =" 3" Fe(s)+ 2O2(g) △H ="b" kJ/mol
则光解气态水制备H2的热化学方程式为__ __。
(2)步骤I中加水发生如下反应,请完善该反应: +2H2O  2H++ H2TiO3↓;
2H++ H2TiO3↓;
该步骤加入铁粉的作用是① ;② 。
(3)步骤Ⅳ生成(NH4)2Fe(SO4)2,其化学反应方程式为_ ___;操作I为 。
(4)已知在潮湿空气中Fe(OH)2比FeCl2更易被氧化。据此分析(NH4)2Fe(SO4)2比FeSO4稳定的原因是 。
填空题 (14分)实验室测量KMnO4溶液浓度时常用(NH4)2Fe(SO4)2代替FeSO4作标液,(NH4)2Fe来源:91考试 网(SO4)2的制备工艺流程如下:

(1)已知流程中铁粉制备反应如下:
4 H2 O(g) +3Fe(s) Fe3O4(s)十4H2(g) △H ="a" kJ /mol
Fe3O4(s)十4H2(g) △H ="a" kJ /mol
Fe3O4(s) =" 3" Fe(s)+ 2O2(g) △H ="b" kJ/mol
则光解气态水制备H2的热化学方程式为__ __。
(2)步骤I中加水发生如下反应,请完善该反应: +2H2O  2H++ H2TiO3↓;
2H++ H2TiO3↓;
该步骤加入铁粉的作用是① ;② 。
(3)步骤Ⅳ生成(NH4)2Fe(SO4)2,其化学反应方程式为_ ___;操作I为 。
(4)已知在潮湿空气中Fe(OH)2比FeCl2更易被氧化。据此分析(NH4)2Fe(SO4)2比FeSO4稳定的原因是 。
本题答案:(1)H2O(g)= H2(g)+1/2O2(g)△H=(a
本题解析:
试题分析:(1)根据盖斯定律可将两个热化学方程式相加后都除以4,所以光解气态水制备H2的热化学方程式为H2O(g)= H2(g)+1/2O2(g)△H=(a+b)/4kJ/mol;
(2)根据质量守恒定律,则反应物为TiO2+;因为该流程的目的是制备硫酸亚铁铵,所以加入铁粉的目的是防止Fe2+氧化为Fe3+,同时步骤I中产生钛酸的沉淀,则加入铁粉可与氢离子反应促进反应正向进行,以除去Ti元素;
(3)步骤II过滤后的滤液为硫酸亚铁溶液,则步骤Ⅳ生成(NH4)2Fe(SO4)2,则硫酸亚铁与硫酸铵反应生成硫酸亚铁铵,化学方程式为(NH4)2SO4+FeSO4=(NH4)2Fe(SO4)2;从溶液中得到晶体的操作为蒸发浓缩、冷却结晶、过滤等,所以操作I是蒸发浓缩、冷却结晶;
(4)已知在潮湿空气中Fe(OH)2比FeCl2更易被氧化,说明二价铁在碱性条件下更易被氧化,(NH4)2Fe(SO4)2溶液中存在亚铁离子和铵根离子的水解,所以水解后的酸性强于FeSO4,则(NH4)2Fe(SO4)2的还原性小于FeSO4,不易被氧化,所以更稳定 。
考点:考查物质的制备流程的分析,盖斯定律的应用,基本操作的判断
本题所属考点:【热化学方程式】
本题难易程度:【一般】
All is not at hand that helps. 世间没有唾手可得之事.