|
|
|
(16分)选择适当的催化剂在高温下可将汽车尾气中的 CO、NO转化为?【热化学方程式】
2016-12-27 00:15:21
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (16分)选择适当的催化剂在高温下可将汽车尾气中的 CO、NO转化为无毒气体。
(1)已知:①2CO(g)+O2(g)=2CO2(g) ?H1="a" kJ?mol-1
②2NO(g)+2CO(g) ?N2(g)+ 2CO2(g) ?H2="b" kJ?mol-1
则反应N2(g)+ O2(g)= 2NO(g)的?H= kJ?mol-1(用a、b表示)。
(2)在一定温度下,向1L密闭容器中充入0.5 mol NO、2 mol CO,发生上述反应②,20S反应达平衡,此时CO的物质的量为1.6 mol。请回答下列问题:
①前20S内平均反应速率v(NO)为 。
②在该温度下反应的平衡常数K= 。
③关于上述反应,下列叙述不正确的是 & #160; (填编号)。
A.达到平衡时,移走部分CO2,平衡将向右移动,正反应速率加快
B.缩小容器的体积,平衡将向右移动
C.在相同的条件下,若使用甲催化剂能使正反应速率加快105倍,使用乙催化剂能使逆反应速率加快108倍,则应该选用乙催化剂
D.若保持平衡时的温度和压强不变,再向容器中充入0.4molCO和0.8mol N2,则此时v正>v逆
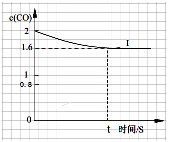
| ④已知上述实验中,c(CO)与反应时间t变化曲线Ⅰ。若其它条件不变,将0.5 mol NO、2 mol CO投入2 L容器进行反应,请在答题卡图中绘出c(CO)与反应时间t1变化曲线Ⅱ。
(3)测试某汽车冷启动时的尾气催化处理CO、NO百分含量随时间变化曲线如下图
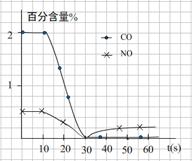
请回答:前0―10 s 阶段,CO、NO百分含量没明显变化的原因是 。
填空题 (16分)选择适当的催化剂在高温下可将汽车尾气中的 CO、NO转化为无毒气体。
(1)已知:①2CO(g)+O2(g)=2CO2(g) ?H1="a" kJ?mol-1
②2NO(g)+2CO(g) ?N2(g)+ 2CO2(g) ?H2="b" kJ?mol-1
则反应N2(g)+ O2(g)= 2NO(g)的?H= kJ?mol-1(用a、b表示)。
(2)在一定温度下,向1L密闭容器中充入0.5 mol NO、2 mol CO,发生上述反应②,20S反应达平衡,此时CO的物质的量为1.6 mol。请回答下列问题:
①前20S内平均反应速率v(NO)为 。
②在该温度下反应的平衡常数K= 。
③关于上述反应,下列叙述不正确的是 (填编号)。
A.达到平衡时,移走部分CO2,平衡将向右移动,正反应速率加快
B.缩小容器的体积,平衡将向右移动
C.在相同的条件下,若使用甲催化剂能使正反应速率加快105倍,使用乙催化剂能使逆反应速率加快108倍,则应该选用乙催化剂
D.若保持平衡时的温度和压强不变,再向容器中充入0.4molCO和0.8mol N2,则此时v正>v逆
|
④已知上述实验中,c(CO)与反应时间t变化曲线Ⅰ。若其它条件不变,将0.5 mol NO、2 mol CO投入2 L容器进行反应,请在答题卡图中绘出c(CO)与反应时间t1变化曲线Ⅱ。

(3)测试某汽车冷启动时的尾气催化处理CO、NO百分含量随时间变化曲线如下图

请回答:前0―10 s 阶段,CO、NO百分含量没明显变化的原因是
来源:91考试网 。
本题答案:(16分)
(1)a-b (2分)
(
本题解析:
试题分析:(1)根据盖斯定律,反应N2(g)+ O2(g)= 2NO(g)的?H=?H1―?H2=(a-b)kJ?mol-1。
(2)①根据三段式进行计算,2NO(g)+2CO(g) ?N2(g)+ 2CO2(g)
初始浓度(mol?L?1) 0.5 2 0 0
转化浓度(mol?L?1) 0.4 0.4 0.2 0.4
平衡浓度(mol?L?1) 0.1 1.6 0.2 0.4
则前20S内平均反应速率v(NO)=0.4mol/L÷20S=0.02mol・L-1・S-1。
②该温度下反应的平衡常数K=0.2×0.42÷(0.12×1.62)=1.25。
③A、达到平衡时,移走部分CO2,生成物浓度减小,平衡将向右移动,反应物浓度逐渐减小,正反应速率减小,故A错误;B、缩小容器的体积,气体的压强增大,平衡将向右移动,故B正确;C、因为催化剂能同等倍数的增大正反应速率和逆反应速率,所以应选用乙催化剂,故C正确;D、若保持平衡时的温度和压强不变,再向容器中充入0.4molCO和0.8mol N2,则浓度商Q=1×0.42÷(0.12×1.62)="4" >K,所以反应向左进行,即v正 < v逆,故D错误。
④将0.5 mol NO、2 mol CO投入2 L容器进行反应,则起始时CO的浓度为1mol?L?1,因为起始浓度变为原反应的1/2,所以反应速率减小,则达到化学平衡的时间变长,因为容积为2L,为原反应的2倍,所以压强减小,平衡向左移动,则c(CO) > 0.8,可画出图像。
(3)催化剂的催化作用需要在一定温度下才能充分体现出来,所以前0―10 s 阶段,CO、NO百分含量没明显变化的原因是:尚未达到催化剂工作温度(或尚未达到反应的温度)。
考点:本题考查盖斯定律的应用、化学反应速率、化学平衡移动及计算、图像的分析及绘制。
本题所属考点:【热化学方程式】
本题难易程度:【困难】
Make yourself necessary to someone. 使自己成为别人需要的人.



