微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (16分)I.一定条件下铁可以和CO2发生反应:
Fe(s)+CO2(g) FeO(s)+CO(g) ;△H>0。1100℃时,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示。
FeO(s)+CO(g) ;△H>0。1100℃时,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示。
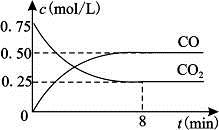
(1)8分钟内,CO的平均反应速率v(CO)=___________(结果保留3位有效数字)。
(2)1100℃时该反应的平衡常数K= (填数值);该温度下,若在8分钟时CO2和CO各增加0.5mol/L,此时平衡 移动(填“正向”、“逆向”或“不”)。
(3)1100℃时,2L的密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
容器
| 甲
| 乙
|
反应物投入量
| 3molFe、2molCO2
| 4molFeO、3molCO
|
CO的浓度(mol/L)
| C1
| C2
|
CO2的体积分数
| φ1
| φ2
|
体系压强(Pa)
| P1
| P2
|
下列说法正确的是___________(填序号);
A.2C1 = 3C2 B.φ1 = φ2 C.P1<P2
II.(4)已知:①Fe(OH)3(aq) Fe3+(aq)+3OH-(aq);ΔH=" a" kJ?mol-1
Fe3+(aq)+3OH-(aq);ΔH=" a" kJ?mol-1
②H2O(l) H+(aq)+OH-(aq);ΔH="b" kJ?mol-1
H+(aq)+OH-(aq);ΔH="b" kJ?mol-1
请写出Fe3+发生水解反应的热化学方程式: 。
(5)柠檬酸(用H3R表示)可用作酸洗剂,除去水垢中的氧化铁。
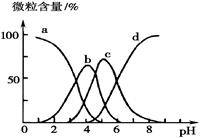
溶液中H3R、H2R-、HR2--、R3-的微粒数百分含量与pH的关系如图所示。图中a曲线所代表的微粒数的百分含量随溶液pH的改变而变化的原因是 (结合必要的方程式解释)。调节柠檬酸溶液的pH=4时,溶液中上述4种微粒含量最多的是 (填微粒符号)。
III.(6)高铁酸钠(Na2FeO4)广泛应用于净水、电池工业等领域,工业常用电解法制备,其原理为
Fe+2OH--+2H2O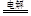 FeO42--+3H2↑
FeO42--+3H2↑
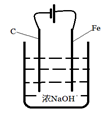
请设计一个电解池并在答题卡的方框内画出该装置的示意图并作相应标注。

其阳极反应式为:________________________________。
填空题 (16分)I.一定条件下铁可以和CO2发生反应:
Fe(s)+CO2(g) FeO(s)+CO(g) △H>0。1100℃时,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示。
FeO(s)+CO(g) △H>0。1100℃时,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示。

(1)8分钟内,CO的平均反应速率v(CO)=___________(结果保留3位有效数字)。
(2)1100℃时该反应的平衡常数K= (填数值);该温度下,若在8分钟时CO2和CO各增加0.5mol/L,此时平衡 移动(填“正向”、“逆向”或“不”)。
(3)1100℃时,2L的密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
容器
| 甲
| 乙
|
反应物投入量
| 3molFe、2molCO2
| 4molFeO、3molCO
|
CO的浓度(mol/L)
| C1
| C2
|
CO2的体积分数
| φ1
| φ2
|
体系压强(Pa)
| P1
| P2
|
下列说法正确的是___________(填序号);
A.2C1 = 3C2 B.φ1 = φ2 C.P1<P2
II.(4)已知:①Fe (OH)3(aq) Fe3+(aq)+3OH-(aq);ΔH=" a" kJ?mol-1
Fe3+(aq)+3OH-(aq);ΔH=" a" kJ?mol-1
②H2O(l) H+(aq)+OH-(aq);ΔH="b" kJ?mol-1
H+(aq)+OH-(aq);ΔH="b" kJ?mol-1
请写出Fe3+发生水解反应的热化学方程式: 。
(5)柠檬酸(用H3R表示)可用作酸洗剂,除去水垢中的氧化铁。
溶液中H3R、H2R-、HR2--、R3-的微粒数百分含量与pH的关系如图所示。图中a曲线所代表的微粒数的百分含量随溶液pH的改变而变化的原因是 (结合必要的方程式解释)。调节柠檬酸溶液的pH=4时,溶液中上述4种微粒含量最多的是 (填微粒符号)。

III.(6)高铁酸钠(Na2FeO4)广泛应用于净水、电池工业等领域,工业常用电解法制备,其原理为
Fe+2OH--+2H2O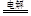 FeO42--+3H2↑
FeO42--+3H2↑
请设计一个电解池并在答题卡的方框内画出该装置的示意图并作相应标注。

其阳极反应式为:________________________________。
本题答案:(1)v(CO)=0.0625mol?L-1?min-1本题解析:
试题分析:(1)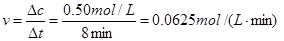 ;
;
(2)K= =
=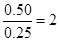 ,该温度下,在8分钟时CO2和CO各增加0.5mol/L,此时平衡正向移动;
,该温度下,在8分钟时CO2和CO各增加0.5mol/L,此时平衡正向移动;
(3)由数据可知,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡,且为等效平衡,达到平衡时,物质的浓度、转化率不随时间的变化而变化,故BC正确;
(4)①Fe(OH)3(aq) Fe3+(aq)+3OH-(aq) ; ΔH=" a" kJ?mol-1
Fe3+(aq)+3OH-(aq) ; ΔH=" a" kJ?mol-1
②H2O(l)  H+(aq)+OH-(aq) ;ΔH=" b" kJ?mol-1
H+(aq)+OH-(aq) ;ΔH=" b" kJ?mol-1
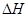 =
=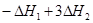 =(3b-a)kJ/mol
=(3b-a)kJ/mol
所以水解的热化学方程式为 Fe3+(aq) +3H2O(l)  Fe(OH)3(aq) +3H+(aq) △H=(3b-a)kJ・mol-1;
Fe(OH)3(aq) +3H+(aq) △H=(3b-a)kJ・mol-1;
(5)溶液中H3R、H2R-、HR2--、R3-的微粒数百分含量与pH的关系可由图可得,图中a曲线所代表的微粒数的百分含量随溶液pH的改变而变化的原因随溶液pH增大,平衡H3R H2R- + H+向右移动,所以,H3R的百分含量减小;调节柠檬酸溶液的pH=4时,溶液显酸性,使H3R
H2R- + H+向右移动,所以,H3R的百分含量减小;调节柠檬酸溶液的pH=4时,溶液显酸性,使H3R H2R- + H+被抑制,平衡逆移,这时含量最多的微粒为H2R-;
H2R- + H+被抑制,平衡逆移,这时含量最多的微粒为H2R-;
(6)由题可知反应原理为Fe+2OH--+2H2O FeO42--+3H2↑,那么阳极为铁,故电极反应为Fe - 6e-+ 8OH-= FeO42-+ 4 H2O,电解池的装置图为
FeO42--+3H2↑,那么阳极为铁,故电极反应为Fe - 6e-+ 8OH-= FeO42-+ 4 H2O,电解池的装置图为
考点:反应速率的计算,平衡常数的计算,平衡移动方向的判断,热化学方程式的书写, 溶液中微粒种类的判断
本题所属考点:【热化学方程式】
本题难易程度:【困难】
False friends are worse than open enemise. 口是心非的朋友比公开的敌人更坏.