微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (13分)碳氧化物、氮氧化物、二氧化硫的处理与利用是世界各国研究的热点问题。
(1)消除汽车尾气中的NO、CO,有利于减少PM2.5的排放。已知如下信息:
I.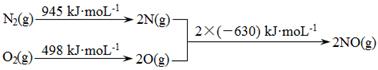
II.N2(g)+ O2(g)  2NO(g) ΔH1
2NO(g) ΔH1
2CO(g) + O2(g) 2CO2 (g) ΔH2=" -565" kJ・mol-1
2CO2 (g) ΔH2=" -565" kJ・mol-1
①ΔH1= 。
②在催化剂作用下NO和CO转化为无毒气体,写出反应的热化学方程式
③一定条件下,单位时间内不同温度下测定的氮氧化物转化率如图1所示。
温度高于710K时,随温度的升高氮氧化物转化率降低的原因可能是
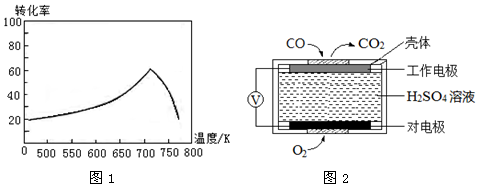
(2)测定汽车尾气常用的方法有两种。
①方法1:电化学气敏传感器法。其中CO传感器的工作原理如图2所示,则工作电极的反应式为
②方法2:氧化还原滴定法。用H2O2溶液吸收尾气,将氮氧化物转化为强酸,用酸碱中和滴定法测定强酸浓度。写出NO与H2O2溶液反应的离子方程式
(3)工业上可以用NaOH溶液或氨水吸收过量的SO2,分别生成NaHSO3、NH4HSO3,其水溶液均呈酸性。相同条件下,同浓度的两种酸式盐的水溶液中c(SO32-)较小的是,用文字和化学用语解释原因 &# 160; 。
填空题 (13分)碳氧化物、氮氧化物、二氧化硫的处理与利用是世界各国研究的热点问题。
(1)消除汽车尾气中的NO、CO,有利于减少PM2.5的排放。已知如下信息:
I.
II.N2(g)+ O2(g)  2NO(g) ΔH1
2NO(g) ΔH1
2CO(g) + O2(g) 2CO2 (g) ΔH2=" -565" kJ・mol-1
2CO2 (g) ΔH2=" -565" kJ・mol-1
①ΔH1= 。
②在催化剂作用下NO和CO转化为无毒气体,写出反应的热化学方程式
③一定条件下,单位时间内不同温度下测定的氮氧化物转化率如图1所示。
温度高于710K时,随温度的升高氮氧化物转化率降低的原因可能是

(2)测定汽车尾气常用的方法有两种。
①方法1:电化学气敏传感器法。其中CO传感器的工作原理如图2所示,则工作电极的反应式为 ;
②方法2:氧化还原滴定法。用H2O2溶液吸收尾气,将氮氧化物转化为强酸,用酸碱中和滴定法测定强酸浓度。写出NO与H2O2溶液反应的离子方程式
(3)工业上可以用NaOH溶液或氨水吸收过量的SO2,分别生成NaHSO3、NH4HSO3,其水溶液均呈酸性。相同条件下,同浓度的两种酸式盐的水溶液中c(SO32-)较小的是,用文字和化学用语解释原因 。
本题答案:(13分,未标分数的空每空2分,合理即给分)
(1)①
本题解析:
试题分析:(1)①化学反应的焓变等于反应物的键能之和减去生成物的键能之和,根据信息Ⅰ中的数据计算反应N2(g)+ O2(g)  2NO(g)的ΔH1=+183kJ・mol-1。②在催化剂作用下NO和CO转化为无毒气体N2和CO2,利用信息II.i N2(g)+ O2(g)
2NO(g)的ΔH1=+183kJ・mol-1。②在催化剂作用下NO和CO转化为无毒气体N2和CO2,利用信息II.i N2(g)+ O2(g)  2NO(g) ΔH1=+183kJ・mol-1,ii 2CO(g) + O2(g)
2NO(g) ΔH1=+183kJ・mol-1,ii 2CO(g) + O2(g) 2CO2 (g) ΔH2=" -565" kJ・mol-1,根据盖斯定律:ii―i得反应的热化学方程式为2CO(g)+2NO(g)
2CO2 (g) ΔH2=" -565" kJ・mol-1,根据盖斯定律:ii―i得反应的热化学方程式为2CO(g)+2NO(g) 2CO2 (g)+N2 (g) ΔH=-748 kJ・mol-1;③温度高于710K时,随温度的升高氮氧化物转化率降低的原因可能是温度升高到710K时,单位时间内反应达平衡,该反应是放热反应,升高温度,平衡向左移动,转化率降低。(2)①CO传感器的工作原理为酸性CO燃料电池,CO发生氧化反应,在原电池的负极参加反应,电极反应式为CO-2e-+H2O
2CO2 (g)+N2 (g) ΔH=-748 kJ・mol-1;③温度高于710K时,随温度的升高氮氧化物转化率降低的原因可能是温度升高到710K时,单位时间内反应达平衡,该反应是放热反应,升高温度,平衡向左移动,转化率降低。(2)①CO传感器的工作原理为酸性CO燃料电池,CO发生氧化反应,在原电池的负极参加反应,电极反应式为CO-2e-+H2O CO2+2H+,O2发生还原反应,作正极,电极反应式为O2+4e-+4H+==2H2O;② NO与H2O2溶液反应生成硝酸和水,离子方程式为2NO+3H2O2
CO2+2H+,O2发生还原反应,作正极,电极反应式为O2+4e-+4H+==2H2O;② NO与H2O2溶液反应生成硝酸和水,离子方程式为2NO+3H2O2 2NO3-+2H2O+2H+;(3)相同条件下,同浓度的NaHSO3、NH4HSO3的水溶液中c(SO32-)较小的是NH4HSO3,原因HSO3-
2NO3-+2H2O+2H+;(3)相同条件下,同浓度的NaHSO3、NH4HSO3的水溶液中c(SO32-)较小的是NH4HSO3,原因HSO3-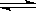 H+ +SO32-,NH4+水解使c(H+)增大,电离平衡逆向移动,c(SO32-)浓度减小。
H+ +SO32-,NH4+水解使c(H+)增大,电离平衡逆向移动,c(SO32-)浓度减小。
考点:考查反应热的计算、盖斯定律,化学平衡,燃料电池及电解质溶液中的离子平衡。
本题所属考点:【热化学方程式】
本题难易程度:【困难】
Call me cousin, but cozen me out. 与我攀亲可以,欺骗我可不行.