|
|
|
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原【燃烧热】
2016-12-27 01:25:52
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 甲醇质子交换膜 燃料电池中将甲醇蒸气转化为氢气的两种反
应原理是 ①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=" +" 49.0 kJ/mol
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ/mol

下列说法正确的是( )
A.CH3OH的燃烧热为192.9 kJ/mol
B.反应①中的能量变化如右图所示
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知:CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g) ΔH > -192.9kJ/mol
|
选择题 甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反
应原理是 ①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=" +" 49.0 kJ/mol
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ/mol

下列说法正确的是( )
A.CH3OH的燃烧热为192.9 kJ/mol
B.反应①中的能量变化如右图所示
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知:CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g) ΔH > -192.9kJ/mol
|
本题答案:D
本题解析:
试题解析:根据盖斯定律将,②×3-①×2可得:CH3OH(g)+
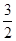
O2(g)=CO2(g)+2H2O(l) △H=-192.9kJ/mol×3-
49kJ/mol×2=-676.7kJ/mol,所以甲醇的燃烧热为676.7kJ/mol,故A错误;反应①的△H>0,而图示的△H=生成物总能量-反应物总能量<0,故B错误;由已知可知,反应①为吸热反应,而反应②为放热反应,故C错误;D、同物质的量的同种物质,气态 能量最高,其次液态能量,固态能量最低,由②推知反应:CH3OH(l)+
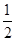
O2(g)=CO2(g)+2H2(g)的△H>-192.9kJ?mol-1,故D正确.
考点:化学能与热能的相互转化
本题所属考点:【燃烧热】
本题难易程度:【一般】
Learn to creep before you leap. Learn to walk before you run. 先学爬,再学跳. 先学走,再学跑.
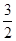 O2(g)=CO2(g)+2H2O(l) △H=-192.9kJ/mol×3-
O2(g)=CO2(g)+2H2O(l) △H=-192.9kJ/mol×3-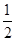 O2(g)=CO2(g)+2H2(g)的△H>-192.9kJ?mol-1,故D正确.
O2(g)=CO2(g)+2H2(g)的△H>-192.9kJ?mol-1,故D正确.