微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (14分)(1)物质的量浓度均为0.1 mol/L的下列溶液:①NH4Cl、②Na2CO3、③NaHCO3、④NaHSO4、⑤CH3COOH、⑥NaOH,pH由大到小的顺为: (填数字代号)
(2)氢气燃烧热值高。实验测得,在常温常压下,1 g H2完全燃烧生成液态水,放出142.9 kJ热量。则H2燃烧的热化学方程式为 _____________________ _____________。
(3)常温下,0.1 mol/L的NaHCO3溶液的pH大于8,则溶液中C(H2CO3)___ _C( CO32-) (填>、=或<),原因_________ ____
(用离子方程式和必要的文字说明)
(4)常温 下,pH=a某强酸溶液V1 L,pH=b某强碱溶液V2 L,已知a+b=12,两溶液混合后pH=7,求V1 和V2的关系
(5)25℃下,某Na2SO4溶液中c(SO42-)=5×10-4 mol・L-1,取该溶液1 mL,加水稀释至10 mL,则稀释后溶液中c (Na+)∶c (OH-)=____ ____
(6)常温下,已知Ksp(Mg(OH)2)=1.8×10-11,则Mg(OH)2在pH=12.00的NaOH溶液中的Mg2+浓度
为 mol・L-1
填空题 (14分)(1)物质的量浓度均为0.1 mol/L的下列溶液:①NH4Cl、②Na2CO3、③NaHCO3、④NaHSO4、⑤CH3COOH、⑥NaOH,pH由大到小的顺为: (填数字代号)
(2)氢气燃烧热值高。实验测得,在常温常压下,1 g H2完全燃烧生成液态水,放出142.9 kJ热量。则H2燃烧的热化学方程式为 _____________________ _____________。
(3)常温下,0.1 mol/L的NaHCO3溶液的pH大于8,则溶液中C(H2CO3)___ _C( CO32-) (填>、=或<),原因_________ ____
(用离子方程式和必要的文字说明)
(4)常温下,pH=a某强酸溶液V1 L,pH=b某强碱溶液V2 L,已知a+b=12,两溶液混合后pH=7,求V1 和V2的关系
(5)25℃下,某Na2SO4溶液中c(SO42-)=5×10-4 mol・L-1,取该溶液1 mL,加水稀释至10 mL,则稀释后溶液中c (Na+)∶c (OH-)=____ ____
(6)常温下,已知Ksp(Mg(OH)2)=1.8×10-11,则Mg(OH)2在pH=12.00的NaOH溶液中的Mg2+浓度
为 mol・L-1
本题答案:(1)⑥②③①⑤④;(2)2H2(g)+O2(g)=2H2O
本题解析:
试题分析:NaHSO4为强酸的酸式盐,c(H+)=0.1mol/L;NaOH为强碱,c(OH―)=0.1mol/L;CH3COOH为弱酸,NaOH的PH最大、NaHSO4的PH最小;NH4Cl水解溶液呈酸性;Na2CO3、NaHCO3水解呈碱性,Na2CO3的水解程度大于NaHCO3,所以PH由大到小的顺为⑥②③①⑤④;(2)2 mol H2完全燃烧生成液态水,放出4×142.9 kJ热量,H2燃烧的热化学方程式为2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ?mol-1;(3)HCO3―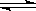 H++ CO32―电离呈酸性、HCO3―+H2O
H++ CO32―电离呈酸性、HCO3―+H2O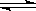 H2CO3+OH-,水解呈碱性,溶液的pH大于8,说明水解大于电离,C(H2CO3)>C( CO32-);(4)
H2CO3+OH-,水解呈碱性,溶液的pH大于8,说明水解大于电离,C(H2CO3)>C( CO32-);(4)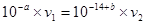 ,
,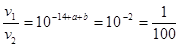 ;(5)c(SO42-)=5×10-4 mol・L-1,c (Na+)=1×10-3 mol・L-1,Na2SO4溶液呈中性,所以c (OH-)= 1×10-7 mol・L-1;c (Na+)∶c (OH-)= 1000:1;(6)pH=12.00的NaOH溶液中c (OH-)= 1×10-2 mol・L-1,
;(5)c(SO42-)=5×10-4 mol・L-1,c (Na+)=1×10-3 mol・L-1,Na2SO4溶液呈中性,所以c (OH-)= 1×10-7 mol・L-1;c (Na+)∶c (OH-)= 1000:1;(6)pH=12.00的NaOH溶液中c (OH-)= 1×10-2 mol・L-1,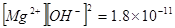 ,所以Mg2+浓度为1.8×10-7mol・L-1。
,所以Mg2+浓度为1.8×10-7mol・L-1。
考点:本题考查水溶液。
本题所属考点:【燃烧热】
本题难易程度:【困难】
Better a glorious death than a shameful life. 宁求光荣死,不可耻辱生.