|
|
|
下列关于热化学方程式和反应的热效应的叙述中,正确的是A.?【燃烧热】
2016-12-27 01:44:35
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 下列关于热化学方程式和反应的热效应的叙述中,正确的是
A.已知2C(s)+2O2(g)=2CO2(g);△H1,2C(s)+O2(g)="2CO(g)" ;△H2。则△H1<△H2
B.500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为: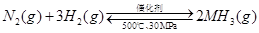 △H=-38.6kJ・mol-1 △H=-38.6kJ・mol-1
C.含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则该条件下稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(aq);△H=-57.4 kJ/mol
D.已知2H2(g)+O2(g)=2H2O(g);△H=-483.6 kJ/mol,则氢气的燃烧热为241.8 k J/mol
|
选择题 下列关于热化学方程式和反应的热效应的叙述中,正确的是
A.已知2C(s)+2O2(g)=2CO2(g);△H1,2C(s)+O2(g)="2CO(g)" ;△H2。则△H1<△H2
B.500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为: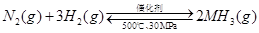 △H=-38.6kJ・mol-1 △H=-38.6kJ・mol-1
C.含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则该条件下稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(aq);△H=-57.4 kJ/mol
D.已知2H2(g)+O2(g)=2H2O(g);△H=-483.6 kJ/mol,则氢气的燃烧热为241.8 kJ/mol
|
本题答案:A
本题解析:
试题分析:A、碳完全燃烧放热多,由于△H小于0,放热越多,△H越小,则根据2C(s)+2O2(g)=2CO2(g);△H1,2C(s)+O2(g)="2CO(g)" ;△H2可知△H1<△H2,A正确;B、500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,由于合成氨反应是可逆反应,因此1mol完全反应放出的热量大于38.6kJ,B错误;C、醋酸是弱酸,电离过程需要吸热,则NaOH(aq)+CH3COOH(aq)
本题所属考点:【燃烧热】
本题难易程度:【一般】
Morale should be boosted, not dampened. 气可鼓而不可泄.