|
|
|
以下说法正确的是()A.某吸热反应能自发进行,因此该反应?【化学反应与能量】
2016-12-27 09:07:41
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 以下说法正确的是()
A.某吸热反应能自发进行,因此该反应是熵增反应
B.常温下Na与足量O2反应生成Na2O随温度升高生成Na2O的速 率逐渐加快
C.放热反应速率总是大于吸热反应速率
D.1gH2完全燃烧生成水蒸气时放出热量为121kJ,完全断裂1mol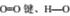 键吸收热量为496kJ、463kJ,则断裂1mol H-H键时吸收热量为902kJ 键吸收热量为496kJ、463kJ,则断裂1mol H-H键时吸收热量为902kJ
|
选择题 以下说法正确的是()
A.某吸热反应能自发进行,因此该反应是熵增反应
B.常温下Na与足量O2反应生成Na2O随温度升高生成Na2O的速率逐渐加快
C.放热反应速率总是大于吸热反应速率
D.1gH2完全燃烧生成水蒸气时放出热量为121kJ,完全断裂1mol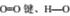 键吸收热量为496kJ、463kJ,则断裂1mol H-H键时吸收热量为902kJ 键吸收热量为496kJ、463kJ,则断裂1mol H-H键时吸收热量为902kJ
|
本题答案:A
本题解析:
试题分析:A. 某吸热反应能自发进行,根据体系的自由能ΔG=ΔH-TΔS<0,可以自发进行可知:该反应是熵增反应,正确;B. 常温下Na与足量O2反应生成Na2O,当温度升高后不仅该反应速率会增加,还会发生反应产生Na2O2,错误;C. 影响化学反应速率的大小的因素有很多,当可逆反应达到平衡时放热反应速率等于吸热反应速率,错误;D. 反应热是断键吸热与成键放热的差值。1gH2完全燃烧生成水蒸气时放出热量为121kJ,若完全断裂1molO=O键、H―O键吸收热量为496kJ、463kJ,则断裂1mol H-H键时吸收热量为[-121kJ×4+(4×463kJ )-496kJ ]÷2=436kJ,错误。
考点:考查反应的自发性、键能与反应热的关系、反应原理与温度及反应的热效应与温度的关系的知识。
本题所属考点:【化学反应与能量】
本题难易程度:【一般】
Fair words fill not the belly. 甜言蜜语填不饱肚子。