|
|
|
碘与氢气反应的热化学方程式为:①I2(g)+H2(g)<img src="htt【化学反应与能量】
2016-12-27 09:47:44
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 碘与氢气反应的热化学方程式为:
①I2(g)+H2(g)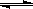 2HI(g) ΔH=" -" 9.48 kJ・mol-1 2HI(g) ΔH=" -" 9.48 kJ・mol-1
②I2(s)+H2(g)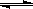 2HI(g) ΔH=" +" 26. 48 kJ・mol-1,由此判断下列说法或反应正确的是 2HI(g) ΔH=" +" 26. 48 kJ・mol-1,由此判断下列说法或反应正确的是
A.反应①的产物比反应②的产物稳定
B.I2(s)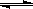 I2(g)ΔH=" +" 17.00 kJ・mol-1 I2(g)ΔH=" +" 17.00 kJ・mol-1
C.反应②的反应物总能量比反应①的反应物总能量低
D.1 mol I2(g)中通入1 mol H2(g),反应后放热9.48 kJ
|
选择题 碘与氢气反应的热化学方程式为:
①I2(g)+H2(g)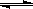 2HI(g) ΔH=" -" 9.48 kJ・mol-1 2HI(g) ΔH=" -" 9.48 kJ・mol-1
②I2(s)+H2(g)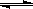 2HI(g) ΔH=" +" 26.48 kJ・mol-1,由此判断下列说法或反应正确的是 2HI(g) ΔH=" +" 26.48 kJ・mol-1,由此判断下列说法或反应正确的是
A.反应①的产物比反应②的产物稳定
B.I2(s)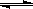 I2(g)ΔH=" +" 17.00 kJ・mol-1 I2(g)ΔH=" +" 17.00 kJ・mol-1
C.反应②的反应物总能量比反应①的反应物总能量低
D.1 mol I2(g)中通入1 mol H2(g),反应后放热9.48 kJ
|
本题答案:C
本题解析:
试题分析:A、同一种物质在相同条件下,能量一样多,A错误;B、利用盖斯定律可得出1 mol固态碘与1 mol气态碘所含的能量相差35.96 kJ,B错误,C项正确;D、反应是可逆反应,反应物不能完全转化,放热达不到9.48 kJ,D错误。答案选C。
考点:考查化学反应热的计算。
本题所属考点:【化学反应与能量】
本题难易程度:【一般】
The world is but a little place,after all. 天涯原咫尺,何处不相逢.