微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (12分)中和热的测定是高中重要的定量实验。取0.55 mol/L的NaOH溶液50 mL与0.50 mol/L的盐酸50 mL置于图所示的装置中进行中和热的测定实验,回答下列问题
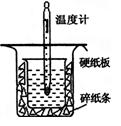
(1)从上图实验装置看,其中尚缺少的一种玻璃用品是_________ _,除此之外,装置中的一个明显错误是 。
(2)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热数值会_________,(填“偏大”、“偏小”或“不变”)。
(3)实验中改用60 mL 0.50 mol・L-1盐酸跟50 mL 0.55 mol・L-1 NaOH溶液进行反应,与上述实验相比,所求中和热 (填“相等”或“不相等”),简述理由: 。
(4)某实验小组用盐酸和氢氧化钠溶液做了三次实验,每次取溶液各50 mL,并记录下原始数据:
实验序号
| 起始温度t1/℃
| 终止温度(t2)/℃
| 温差(t2-t1)/℃
|
盐酸
| NaOH溶液
| 平均值
|
1
| 25.1
| 24.9
| 25.0
| 28.3
| 3.3
|
2
| 25.1
| 25.1
| 25.1
| 28.6
| 3.5
|
3
| 25.1
| 25.1
| 25.1
| 27.1
| 2.0
|
已知盐酸、NaOH溶液密度近似 为1.00 g/cm3,中和后混合液的比热容c=4.18×10-3 kJ/(g・℃),根据计算结果,写出该中和反应的热化学方程式 。
填空题 (12分)中和热的测定是高中重要的定量实验。取0.55 mol/L的NaOH溶液50 mL与0.50 mol/L的盐酸50 mL置于图所示的装置中进行中和热的测定实验,回答下列问题

(1)从上图实验装置看,其中尚缺少的一种玻璃用品是_________ _,除此之外,装置中的一个明显错误是 91ExaM.org 。
(2)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热数值会_________,(填“偏大”、“偏小”或“不变”)。
(3)实验中改用60 mL 0.50 mol・L-1盐酸跟50 mL 0.55 mol・L-1 NaOH溶液进行反应,与上述实验相比,所求中和热 (填“相等”或“不相等”),简述理由: 。
(4)某实验小组用盐酸和氢氧化钠溶液做了三次实验,每次取溶液各50 mL,并记录下原始数据:
实验序号
| 起始温度t1/℃
| 终止温度(t2)/℃
| 温差(t2-t1)/℃
|
盐酸
| NaOH溶液
| 平均值
|
1
| 25.1
| 24.9
| 25.0
| 28.3
| 3.3
|
2
| 25.1
| 25.1
| 25.1
| 28.6
| 3.5
|
3
| 25.1
| 25.1
| 25.1
| 27.1
| 2.0
|
已知盐酸、NaOH溶液密度近似为1.00 g/cm3,中和后混合液的比热容c=4.18×10-3 kJ/(g・℃),根据计算结果,写出该中和反应的热化学方程式 。
本题答案:
(1)环形玻璃搅拌棒;小烧杯口未用硬纸板盖住(或大烧
本题解析:
试题分析:测定中和热应尽量减少热量的损失,且使酸与碱快速充分反应,(1)从装置图可以看出缺少环形玻璃搅拌棒;小烧杯口未用硬纸板盖住(或大烧杯内碎纸条塞少了,未将小烧杯垫的足够高)会造成热量的损失。(2)醋酸是弱酸,电离过程会吸收热量,则测得的中和热数值会偏小;(3)中和热是指中和生成1 mol H2O所放出的热量(与所用酸、碱的用量无关);(4)分析三组数据,舍去第3组数据,取前两组数据的平均值进行计算,反应生成水的物质的量为0.050L×0.5m ol/L=0.025mol,放出的热量为Q=3.4℃×100g×4.18×10-3 kJ/(g・℃)=1.4212KJ,则中和热△H=-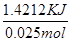 =-56.85 KJ/mol.
=-56.85 KJ/mol.
考点:中和热的测定
本题所属考点:【化学反应与能量】
本题难易程度:【一般】
Laziness in youth spells regret in old age. 少壮不努力,老大徒伤悲.