|
|
|
下列说法正确的是<img src="http://www.91exam.org/91files/【化学反应与能量】
2016-12-27 09:55:29
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 下列说法正确的是
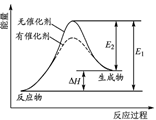
A.某反应的反应过程中能量变化如图所示,由上图分析可知催化剂不改变反应的焓变
B.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快
C.已知: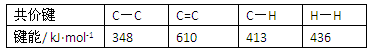 则可以计算出反应 则可以计算出反应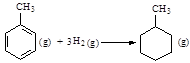 的ΔH为-384 kJ・mol-1 的ΔH为-384 kJ・mol-1
D.常温下在0.10 mol・L-1的氨水中加入少量NH4Cl晶体,NH3・H2O的电离程度和溶液的pH均减小
|
91eXaM.org
选择题 下列说法正确的是

A.某反应的反应过程中能量变化如图所示,由上图分析可知催化剂不改变反应的焓变
B.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快
C.已知: 则可以计算出反应 则可以计算出反应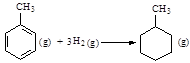 的ΔH为-384 kJ・mol-1 的ΔH为-384 kJ・mol-1
D.常温下在0.10 mol・L-1的氨水中加入少量NH4Cl晶体,NH3・H2O的电离程度和溶液的pH均减小
|
本题答案:AD
本题解析:
试题分析:A.由于催化剂能够降低反应的活化能但是不变改变反应物与生成物的能力差,及不能改变焓变
91exam.org,正确;B.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快,反应原理也会发生改变,Na与O2反应生成Na2O2,错误;C.由于在苯环内含有的化学键不是碳碳单键与碳碳双键的交替结构,而是介于单键和双键之间的一种独特的化学键,所以根据表格的键能大小不能确定该反应的反应热,错误;D. 在氨水中存在电离平衡:NH3・H2O
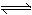
NH4++OH-;若向氨水中加入少量NH4Cl晶体,平衡逆向移动,NH3・H2O的电离程度减小,由于c(OH-)减小,所以溶液的pH也减小,正确。
考点:考查反应热与焓变和键能的关系、温度对反应速率反应原理的影响、微粒浓度对弱电解质电离平衡的影响的知识。
本题所属考点:【化学反应与能量】
本题难易程度:【一般】
It is a long lane that has no turning. 路长有弯,事长有变。
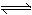 NH4++OH-;若向氨水中加入少量NH4Cl晶体,平衡逆向移动,NH3・H2O的电离程度减小,由于c(OH-)减小,所以溶液的pH也减小,正确。
NH4++OH-;若向氨水中加入少量NH4Cl晶体,平衡逆向移动,NH3・H2O的电离程度减小,由于c(OH-)减小,所以溶液的pH也减小,正确。