|
|
|
FeS与一定浓度的HNO3反应,生成Fe(NO3)3、Fe2(SO4)3、NO2、N2O4?【有关氧化还原反应的计算】
2016-12-27 12:17:31
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 FeS与一定浓度的HNO3反应,生成Fe(NO3)3、Fe2(SO4)3、NO2、N2O4、NO和H2O,当 NO2、N2O4、NO的物质的量之比为1:1:1时,实际参加反应的FeS与HNO3的物质的量之比为
A.1:6
B.2:15
C.2:11
D.1:7
|
选择题 FeS与一定浓度的HNO3反应,生成Fe( NO3)3、Fe2(SO4)3、NO2、N2O4、NO和H2O,当NO2、N2O4、NO的物质的量之比为1:1:1时,实际参加反应的FeS与HNO3的物质的量之比为
A.1:6
B.2:15
C.2:11
D.1:7
|
本题答案:D
本题解析:设生成NO2、N2O4、NO的物质的量均为1mol,则被还原的HNO3物质的量为4mol,共得到6mol电子;1molFeS在反应中失去9mol电子,故被氧化的FeS物质的量为mol,生成物中 Fe2(SO4)3的物质的量是
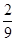
mol,Fe(NO3)3的物质的量也是
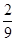
×(
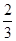
-
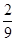
×2)mol,即反应中有
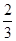
mol HNO3生成了盐,因此共有
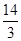
mol HNO3参加反应,实际参加反应的FeS与HNO3的物质的量之比为
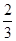
mol:
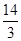
mol =1:7,D正确。
本题所属考点:【有关氧化还原反应的计算】
本题难易程度:【一般】
Judge not of men and things at first sight. 不要靠初次的印象来判断人或事。
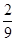 mol,Fe(NO3)3的物质的量也是
mol,Fe(NO3)3的物质的量也是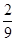 ×(
×(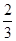 -
-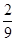 ×2)mol,即反应中有
×2)mol,即反应中有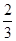 mol HNO3生成了盐,因此共有
mol HNO3生成了盐,因此共有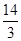 mol HNO3参加反应,实际参加反应的FeS与HNO3的物质的量之比为
mol HNO3参加反应,实际参加反应的FeS与HNO3的物质的量之比为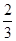 mol:
mol: 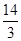 mol =1:7,D正确。
mol =1:7,D正确。